题目内容
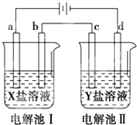 如图所示的电解池I和Ⅱ中,a、b、c和d均为Pt电极.电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b>d.符合上述实验结果的盐溶液是( )
如图所示的电解池I和Ⅱ中,a、b、c和d均为Pt电极.电解过程中,电极b和d上没有气体逸出,但质量均增大,且增重b>d.符合上述实验结果的盐溶液是( )| 选项 | X | Y |
| A | MgSO4 | CuSO4 |
| B | AgNO3 | Pb(NO3)2 |
| C | FeSO4 | Al2(SO4)3 |
| D | AgNO3 | CuSO4 |
| A、A | B、B | C、C | D、D |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:依据装置图分析电极名称a为阳极,b为阴极,c为阳极,d为阴极,结合电解原理,溶液中离子放电顺序分析判断电极反应,电极b和d上没有气体逸出,但质量均增大,说明阴极上溶液中金属离子在阴极析出金属单质,对选项分析判断.
解答:
解:装置图分析电极名称a为阳极,b为阴极,c为阳极,d为阴极,结合电解原理,溶液中离子放电顺序分析判断电极反应,电极b和d上没有气体逸出,但质量均增大,说明阴极上溶液中金属离子在阴极析出金属单质;
A、X为MgSO4,阴极电极反应为溶液中氢离子放电,无金属析出;Y为CuSO4 ,溶液中阴极上铜离子得到电子析出金属,故A错误;
B、X为AgNO3,阴极电极反应为溶液中银离子放电,电极反应为:Ag++e-=Ag,Y为Pb(NO3)2 ,阴极上溶液中氢离子放电,无金属析出,故B错误;
C、X为FeSO4,阴极是溶液中氢离子得到电子生成氢气,无金属析出,Y为Al2 (SO4)3,阴极上是氢离子放电无金属析出,故C错误;
D、Y为CuSO4,阴极是溶液中铜离子析出,电极反应Cu2++2e-=Cu,X为AgNO3,阴极电极反应为溶液中银离子放电,电极反应为:Ag++e-=Ag,依据电子守恒Cu~2Ag,增重b>d,符合题意,故D正确.
故选D.
A、X为MgSO4,阴极电极反应为溶液中氢离子放电,无金属析出;Y为CuSO4 ,溶液中阴极上铜离子得到电子析出金属,故A错误;
B、X为AgNO3,阴极电极反应为溶液中银离子放电,电极反应为:Ag++e-=Ag,Y为Pb(NO3)2 ,阴极上溶液中氢离子放电,无金属析出,故B错误;
C、X为FeSO4,阴极是溶液中氢离子得到电子生成氢气,无金属析出,Y为Al2 (SO4)3,阴极上是氢离子放电无金属析出,故C错误;
D、Y为CuSO4,阴极是溶液中铜离子析出,电极反应Cu2++2e-=Cu,X为AgNO3,阴极电极反应为溶液中银离子放电,电极反应为:Ag++e-=Ag,依据电子守恒Cu~2Ag,增重b>d,符合题意,故D正确.
故选D.
点评:本题考查了电解原理的分析应用,主要是电极反应,溶液中离子浓度放电顺序的判断,电极反应书写方法和电子守恒的计算应用,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
配制100mL 0.100mol/L Na2CO3溶液时,有下列步骤:①溶解 ②转移 ③定容 ④计算 ⑤称量 ⑥洗涤,正确的顺序为( )
| A、⑤④①⑥②③ |
| B、⑤④②①⑥③ |
| C、④⑤①②⑥③ |
| D、⑥④③⑤①② |
25℃时,相同物质的量浓度的下列溶液:①NaCl ②NaOH ③H2SO4 ④(NH4)2SO4,其中水的电离程度按由大到小顺序排列的一组是( )
| A、④>③>②>① |
| B、②>③>①>④ |
| C、④>①>②>③ |
| D、③>②>①>④ |
下列有关化学基本概念的叙述正确的是( )
| A、SiO2和Al2O3都既能与酸反应,又能与碱反应,均属于两性氧化物 |
| B、根据不同的分类标准,NaOH可归类为强碱、纯碱、强电解质等 |
| C、葡萄糖、淀粉和氨基酸在一定条件下都能发生水解反应 |
| D、水结冰时体积膨胀,密度减小,是因为水分子大范围以氢键相连,形成疏松晶体 |
已知常温时红磷转化为白磷时需吸收热量,在下列反应中若a、b均大于零,则a和b的关系为( )
P4(白磷,s)+5O2(g)═2P2O5(s);△H=-a kJ?mol-1
4P(红磷,s)+5O2(g)═2P2O5(s);△H=-b kJ?mol-1.
P4(白磷,s)+5O2(g)═2P2O5(s);△H=-a kJ?mol-1
4P(红磷,s)+5O2(g)═2P2O5(s);△H=-b kJ?mol-1.
| A、a<b | B、a=b |
| C、a>b | D、无法确定 |
取不同质量的某种镁粉和铜粉的均匀混合物分别与相同浓度的盐酸充分反应,实验数据记录如下表则该盐酸的物质的量浓度为(mol?L-1)( )
| 实验序号 | (1) | (2) | (3) |
| 取用盐酸的体积/mL | 25 | 25 | 25 |
| 取用混合物的质量/g | 1.32 | 1.54 | 2.20 |
| 生成气体的体积(标准状况)/mL | 336 | 392 | 448 |
| A、1.2 | B、1.4 |
| C、1.6 | D、无法计算 |
下列热化学方程式书写正确的是( )
| A、MgCO3(s)═MgO(s)+CO2(g)△H=+114.7 |
| B、CO(g)+2H2(g)═CH3OH(l)△H=-128.1 KJ/mol |
| C、C+O2═CO2 △H=+393.5 kJ/mol |
| D、2H2(g)+O2(g)═2H2O△H=-483.6 kJ?mol-1 |
甲烷、乙烯、苯、乙醇是常见的有机物,下列关于其性质说法中正确的是( )
| A、这四种有机化合物都是烃 |
| B、乙烯是一种重要的化工原料,可以用于合成乙醇 |
| C、苯分子中含有不饱和键,因此它与乙烯的性质相似,能使酸性高锰酸钾溶液褪色 |
| D、这四种有机化合物都能燃烧,而且燃烧产物都是二氧化碳和水 |
对化学方程式C+2CuO
2Cu+CO2↑理解不正确的是( )
| ||
| A、木炭与氧化铜在高温下反应生成铜和二氧化碳 |
| B、12份质量的碳可与160份质量的氧化铜在高温下反应生成128份质量的铜和44份质量的二氧化碳 |
| C、若以NA代表6.02×1023个粒子,则NA个碳原子与2NA个氧化铜分子在高温下反应,生成2NA个铜原子和NA个二氧化碳分子 |
| D、一个碳原子和两个氧化铜分子高温加热时可生成两个铜原子和一个二氧化碳分子 |