题目内容
Ⅰ.甲图是几种实验中常用的仪器:写出序号所代表的仪器的名称:
A ;B ;C ; D .
Ⅱ.实验室要配制480mL 0.2mol/L NaOH溶液,请回答下列问题:
(1)配制过程中不需要使用的化学仪器有 (填选项的字母).
A.烧杯 B.500mL容量瓶 C.漏斗 D.胶头滴管 E.玻璃棒
(2)用托盘天平称取氢氧化钠,其质量为 g.
(3)取用任意体积的该NaOH溶液时,下列物理量中不随所取体积的多少而变化的是 .
A.溶液中NaOH的物质的量 B.溶液的浓度 C.溶液中OH-的数目 D.溶液的密度.

A
Ⅱ.实验室要配制480mL 0.2mol/L NaOH溶液,请回答下列问题:
(1)配制过程中不需要使用的化学仪器有
A.烧杯 B.500mL容量瓶 C.漏斗 D.胶头滴管 E.玻璃棒
(2)用托盘天平称取氢氧化钠,其质量为
(3)取用任意体积的该NaOH溶液时,下列物理量中不随所取体积的多少而变化的是
A.溶液中NaOH的物质的量 B.溶液的浓度 C.溶液中OH-的数目 D.溶液的密度.
考点:配制一定物质的量浓度的溶液
专题:
分析:Ⅰ.根据图示仪器构造写出仪器ABCD的名称;
Ⅱ.(1)配制480mL溶液,需要选用500mL容量瓶,根据配制 500mL0.2mol/L NaOH溶液的步骤选择使用的仪器;
(2)根据n=cV计算出500mL0.2mol/L NaOH溶液中溶质的物质的量,再根据m=nM计算出氢氧化钠的质量;
(3)溶液为均一稳定的混合物,所以溶液的物质的量浓度、密度不受体积影响,而氢氧化钠的物质的量、溶液中氢氧根离子数目与溶液体积有关.
Ⅱ.(1)配制480mL溶液,需要选用500mL容量瓶,根据配制 500mL0.2mol/L NaOH溶液的步骤选择使用的仪器;
(2)根据n=cV计算出500mL0.2mol/L NaOH溶液中溶质的物质的量,再根据m=nM计算出氢氧化钠的质量;
(3)溶液为均一稳定的混合物,所以溶液的物质的量浓度、密度不受体积影响,而氢氧化钠的物质的量、溶液中氢氧根离子数目与溶液体积有关.
解答:
Ⅰ.根据图示仪器的构造可知,A仪器为漏斗、B为1000mL容量瓶、C为冷凝管、D为分液漏斗,
故答案为:漏斗;1000mL容量瓶;冷凝管;分液漏斗;
Ⅱ.(1)实验室要配制480mL 0.2mol/L NaOH溶液,实验室中没有480mL的容量瓶,需要选用规格为500mL的容量瓶,实际上配制的溶液为500mL 0.2mol/L NaOH溶液,配制步骤为:计算、称量、溶解、冷却、转移、洗涤、定容、摇匀等,使用的仪器为:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,所以不会使用的仪器为:C漏斗,
故答案为:C;
(2)500mL 0.2mol/L NaOH溶液中含有氢氧化钠的物质的量为:0.2mol/L×0.5L=0.1mol,需要氢氧化钠的质量为:40g/mol×0.1mol=4.0g,
故答案为:4.0;
(3)A.根据n=cV可知,溶液中NaOH的物质的量与溶液体积大小有关,故A错误;
B.溶液具有均一性,所以氢氧化钠溶液的浓度与溶液的体积大小没有关系,故B正确;
C.溶液中OH-的数目与氢氧化钠的物质的量有关,根据n=cV可知,氢氧根离子的数目与溶液的体积大小有关,故C错误;
D.溶液为均一、稳定的混合物,所以溶液的密度与溶液体积大小无关,故D正确;
故选BD.
故答案为:漏斗;1000mL容量瓶;冷凝管;分液漏斗;
Ⅱ.(1)实验室要配制480mL 0.2mol/L NaOH溶液,实验室中没有480mL的容量瓶,需要选用规格为500mL的容量瓶,实际上配制的溶液为500mL 0.2mol/L NaOH溶液,配制步骤为:计算、称量、溶解、冷却、转移、洗涤、定容、摇匀等,使用的仪器为:托盘天平、药匙、烧杯、玻璃棒、500mL容量瓶、胶头滴管,所以不会使用的仪器为:C漏斗,
故答案为:C;
(2)500mL 0.2mol/L NaOH溶液中含有氢氧化钠的物质的量为:0.2mol/L×0.5L=0.1mol,需要氢氧化钠的质量为:40g/mol×0.1mol=4.0g,
故答案为:4.0;
(3)A.根据n=cV可知,溶液中NaOH的物质的量与溶液体积大小有关,故A错误;
B.溶液具有均一性,所以氢氧化钠溶液的浓度与溶液的体积大小没有关系,故B正确;
C.溶液中OH-的数目与氢氧化钠的物质的量有关,根据n=cV可知,氢氧根离子的数目与溶液的体积大小有关,故C错误;
D.溶液为均一、稳定的混合物,所以溶液的密度与溶液体积大小无关,故D正确;
故选BD.
点评:本题考查了实验室中常见仪器名称、配制一定物质的量浓度的溶液的方法,题目难度不大,注意熟悉实验室中常见仪器的构造及使用方法,掌握配制一定物质的量浓度的溶液的方法;(3)为易错点,注意溶液的性质.

练习册系列答案
相关题目
下列反应的离子方程式书写正确的是( )
| A、氧化镁与稀硫酸反应:MgO+2H+=Mg2++H2O |
| B、碳酸钙和稀盐酸反应:2H++CO32-=CO2↑+H2O |
| C、氯气和氯化亚铁溶液反应:Cl2+Fe2+=Fe3++2Cl- |
| D、铜和稀硝酸反应:Cu+2H+=Cu2++H2↑ |
 某课外兴趣小组用如图装置进行实验,试回答:
某课外兴趣小组用如图装置进行实验,试回答: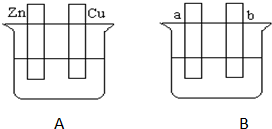
 现有A、B、C、D四种溶液,在进行焰色反应时,火焰颜色都为黄色,它们之间转化关系如图所示.已知B为NaHCO3,请回答下列问题:
现有A、B、C、D四种溶液,在进行焰色反应时,火焰颜色都为黄色,它们之间转化关系如图所示.已知B为NaHCO3,请回答下列问题: