题目内容
6. CO2是一种温室气体,据科学家预测,到21世纪中叶,全球气温将升高1.5-4.5℃,地球气温的升高会引起海平面升高,对人类的生存环境产生巨大的影响.如何合理地利用CO2是摆在科学家面前的一个重大课题.回答下列问题:
CO2是一种温室气体,据科学家预测,到21世纪中叶,全球气温将升高1.5-4.5℃,地球气温的升高会引起海平面升高,对人类的生存环境产生巨大的影响.如何合理地利用CO2是摆在科学家面前的一个重大课题.回答下列问题:(1)工业上利用高温、高压条件,可用CO2与NH3合成尿素[CO(NH2)2],该反应的化学方程式为CO2+NH3 $\frac{\underline{\;高温高压\;}}{\;}$CO(NH2)2+H2O.
(2)一定条件下,不同量的CO2与不同量的NaOH充分反应放出的热景如下表所示:
| CO2的量 | NaOH溶液的量 | 放出的热量 | |
| ① | 22.0g | 750mL1.0mol•L-1 | xkJ |
| ② | 1.0mol | 2.0mL1.0mol•L-1 | ykJ |
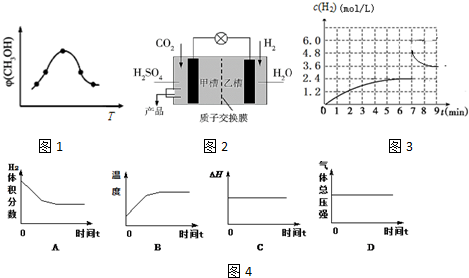
(3)在一定温度和催化剂作用下,可将CO2转化为燃料CH4,反应方程式为CO2(g)+4H2(g)?CH4(g)+2H2O(g)△H. 300℃时,一定量的CO2和H2混合气体在容积为2L的恒容密闭容
器中发生上述反应,5min后达到平衡,此时各物质的浓度如下表:
| 物质 | CO2(g) | H2(g) | CH4(g) | H2O(g) |
| 浓度/mol•L-1 | 0.2 | 0.8 | a | 1.6 |
(4)CO2还可用于生产甲醇,一定条件下,发生反应CO2 (g)+3H(g)?CH3OH(g)+H2O(g)△H.①在容积为2L的恒容密闭容器中,通入2molCO2和3mol H2发生上述反应,下铡碳法能够表明该可逆反应达到平衡状态的是de(填字母).
a.消耗3mol H2(g)时,有lmol CH3OH(g)生成
b.转移3mol电子时,反应的CO2为11.2L(标准状况)
c.体系中气体的密度不变
d.水蒸气的体积分数保持不变
e.单位时间内生成H2(g)与生成H2O(g)的物质的量之比为3:1
②用多孔石墨作电极,30% KOH溶液作电解质溶液,可设计如图甲所示的甲醇燃料电池,该电池的负极反应式为CH3OH-6e-+8OH-═CO32-+6H2O.若将该燃料电池与电解饱和食盐水的装置进行串联(如图),当有0.12mol电子发生转移时,断开电源,将溶液冷却至室温,测得食盐溶液为120mL,则此时乙装置中溶液的pH=14假设食盐水中有足量的NaCl,且Cl2完全逸出).
分析 (1)工业上利用高温、高压条件,可用CO2与NH3合成尿素[CO(NH2)2],该反应的化学方程式为:
CO2+NH3 $\frac{\underline{\;高温高压\;}}{\;}$CO(NH2)2+H2O;
(2)根据题意可知,22gCO2通入1mol•L-1NaOH溶液750mL中充分反应,测得反应放出xkJ的热量,写出热化学反应方程式,再利用1mol CO2通入2mol•L-1NaOH溶液2L中充分反应放出y kJ的热量写出热化学反应方程式,最后利用盖斯定律来书写CO2与NaOH溶液反应生成NaHCO3的热化学方程式;
(3)根据生成物水的浓度可得甲烷的浓度,则n(CH4)=c(CH4)×V,v(CH4)=$\frac{△c(CH4)}{△t}$,再根据化学平衡常数概念计算300℃时的K,根据温度对化学平衡的影响与500℃时该反应的平衡常数K比较可得反应的△H;
(4)①根据化学平衡状态时正逆反应速率相等,各组分含量保持不变分析;
②甲醇的电极为负极,甲醇失电子,甲醇燃烧生成 CO2,CO2在氢氧化钾溶液中以KCO3形式存在,因此负极电极式为CH3OH-6e-+8OH-═CO32-+6H2O;根据转移的电子数计算乙装置中氢离子浓度,可得pH.
解答 解:(1)工业上利用高温、高压条件,可用CO2与NH3合成尿素[CO(NH2)2],该反应的化学方程式为:CO2+NH3 $\frac{\underline{\;高温高压\;}}{\;}$CO(NH2)2+H2O;
故答案为:CO2+NH3 $\frac{\underline{\;高温高压\;}}{\;}$CO(NH2)2+H2O;
(2)根据题意,22gCO2通入1mol•L-1NaOH溶液750mL中充分反应,n(CO2)=22g÷44g/mol=0.5mol,n(NaOH)=1mol•L-1×0.75L=0.75mol,该反应既生成碳酸钠又生成碳酸氢钠,方程式为2CO2+3NaOH═NaHCO3+Na2CO3+H2O,由0.5molCO2反应放出热量为xKJ,则2molCO2反应放出热量为4xKJ,即热化学反应方程式为①2CO2(g)+3NaOH(aq)═NaHCO3 (aq)+Na2CO3(aq)+H2O(l)△H=-4xKJ/mol,又1mol CO2通入2mol•L-1NaOH溶液2L中充分反应放出y kJ的热量,则热化学方程式为②2NaOH(aq)+CO2(g)═Na2CO3(aq)+H2O(l)△H=-yKJ/mol,由盖斯定律可知,①-②可得,NaOH(aq)+CO2(g)═NaHCO3(aq)△H=-(4x-y)KJ/mol;
故答案为:NaOH(aq)+CO2(g)═NaHCO3(aq)△H=-(4x-y)KJ/mol;
(3)由表可知,300℃时,c(H2O)=1.6mol/L,则c(CH4)=$\frac{1}{2}$c(H2O)=0.8mol/L,n(CH4)=0.8mol/L×2L=1.6mol;v(CH4)=$\frac{0.8mol/L}{5min}$=0.16mol/(L•min);300℃时该反应的化学平衡常数K=$\frac{1.{6}^{2}×0.8}{0.2×0.{8}^{4}}$=25,500℃时该反应的平衡常数K=16,说明温度升高,平衡逆向移动,说明反应是个放热反应,△H<0;
故答案为:1.6mol;0.16mol/(L•min);<;
(4)①反应CO2 (g)+3H2(g)?CH3OH(g)+H2O(g):
a.无论反应进行到何种时候,都有消耗3mol H2(g)时有lmol CH3OH(g)生成,故a错误;
b.任何时刻转移3mol电子时,反应的CO2均为11.2L(标准状况),故b错误;
c.混合气体的总质量不变,恒容容器混合气体的体积不变,则体系中气体的密度一直不变,故c错误;
d.随着反应的进行,水蒸气的体积分数增大,平衡时,保持不变,故d正确;
e.单位时间内生成H2(g)与生成H2O(g)的物质的量之比为3:1,说明正你反应速率相等,反应平衡,故e正确;
故答案为:de;
②甲醇的电极为负极,甲醇失电子,甲醇燃烧生成 CO2,CO2在氢氧化钾溶液中以KCO3形式存在,因此负极电极式为CH3OH-6e-+8OH-═CO32-+6H2O;乙装置中阴极的反应为2H2O+2e-=H2↑+2OH-,0.12mol电子发生转移,则生成的氢氧根离子也为0.12mol,c(OH-)=$\frac{0.12mol}{0.12L}$=1mol/L,故c(H+)=$\frac{Kw}{c(O{H}^{-})}$=$\frac{1{0}^{-14}}{1}$=10-14,则pH=-lgc(H+)=14;
故答案为:CH3OH-6e-+8OH-═CO32-+6H2O;14.
点评 本题考查热化学方程式的书写和计算,化学平衡状态的判断及有关计算、电化学的电极反应式及计算,题目难度不大,是高考常见题型,注意掌握基础、电化学中计算根据电子守恒的计算方法.

 名校课堂系列答案
名校课堂系列答案| A. | ⑥⑤②①④③ | B. | ⑤⑥②①③④ | C. | ④③②①⑤⑥ | D. | ④③①②⑥⑤ |

| A. | 保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 | |
| B. | 保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均减少 | |
| C. | 保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) | |
| D. | 保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C 的体积分数的2倍 |