题目内容
5.现有常温下pH=a的NaOH溶液与pH=b的硫酸溶液,将二者等体积混合,所得溶液为中性,则下列对两溶液的相关分析不正确是( )| A. | KW均为1×10-14 | B. | 若a=12则b=2 | ||
| C. | a、b为固定值 | D. | 水电离出的c(H+)相等 |
分析 常温下pH=a的NaOH溶液与pH=b的硫酸溶液,将二者等体积混合,所得溶液为中性,说明氢离子与氢氧根离子恰好反应,
A.水的离子积只与温度有关;
B.氢离子与氢氧根离子的浓度相同;
C.10-a×10-b=1×10-14;
D.氢离子与氢氧根离子的浓度相同,对水的电离的抑制程度相同.
解答 解:常温下pH=a的NaOH溶液与pH=b的硫酸溶液,将二者等体积混合,所得溶液为中性,说明氢离子与氢氧根离子恰好反应,
A.水的离子积只与温度有关,常温下KW均为1×10-14,故A正确;
B.氢离子与氢氧根离子恰好反应,氢离子与氢氧根离子的浓度相同,所以若a=12,c(OH-)=10-2mol/L,则b=2,c(H+)=10-2mol/L,故B正确;
C.氢离子与氢氧根离子的浓度相同,则10-a×10-b=1×10-14,所以a+b=14,则a、b的值不固定,故C错误;
D.氢离子与氢氧根离子的浓度相同,对水的电离的抑制程度相同,所以水电离出的c(H+)相等,故D正确.
故选C.
点评 本题考查酸碱混合溶液定性判断,明确溶液中溶质及其性质是解本题关键,注意:酸或碱抑制水电离,氢离子与氢氧根离子浓度相同对水的电离抑制程度相同,题目难度不大.

练习册系列答案
相关题目
13.下列化学用语正确的是( )
| A. | 氮分子的电子式: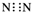 | B. | 溴化钠的电子式: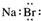 | ||
| C. | 硫原子的结构示意图: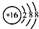 | D. | 水分子的结构式: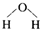 |
10.用Pt做电极电解100moLCuSO4溶液,电解一段时间后两极均收集到标准状况下的气体2.24L,则下列有关说法错误的是( )
| A. | 原CuSO4溶液的浓度为1mol/L | |
| B. | 若要使电解后的溶液恢复至电解前的CuSO4溶液,则需加入9.8gCu(OH)2固体 | |
| C. | 电解过程中转移电子数为0.4NA个 | |
| D. | 假设电解过程中忽略溶液体积变化,则电解后所得溶液中C(H+)=0.1mol/L |
6.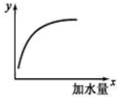 如图表示 25℃时,向 1L,0.1mol•L-1的一元弱酸HA中加水稀释过程的变化图象,则图中纵坐标y表示的是( )
如图表示 25℃时,向 1L,0.1mol•L-1的一元弱酸HA中加水稀释过程的变化图象,则图中纵坐标y表示的是( )
 如图表示 25℃时,向 1L,0.1mol•L-1的一元弱酸HA中加水稀释过程的变化图象,则图中纵坐标y表示的是( )
如图表示 25℃时,向 1L,0.1mol•L-1的一元弱酸HA中加水稀释过程的变化图象,则图中纵坐标y表示的是( )| A. | c(H+)或 c(OH-) | B. | HA的电离平衡常数Ka | ||
| C. | c(H+)/c(HA) | D. | n(H+)或 n(OH-) |
3.25℃,101k Pa时,强酸与强碱的稀溶液发生中和反应生成1mol水时所放出的热量约为57.3kJ/mol;辛烷的燃烧热为5518kJ/mol.下列热化学方程式书写正确的是( )
| A. | CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(l)△H=-57.3kJ/mol | |
| B. | KOH(aq)+$\frac{1}{2}$H2SO4(aq)═$\frac{1}{2}$K2SO4(aq)+H2O(l)△H=-57.3kJ/mol | |
| C. | C8H18(l)+$\frac{25}{2}$ O2 (g)═8CO2 (g)+9H2O(g)△H=-5518 kJ/mol | |
| D. | 2C8H18(g)+25O2 (g)═16CO2 (g)+18H2O(1)△H=-5518 kJ/mol |
4.下列物质中.pH最小的是( )
| A. | 食盐水 | B. | 食醋 | C. | 石灰水 | D. | 纯净水 |
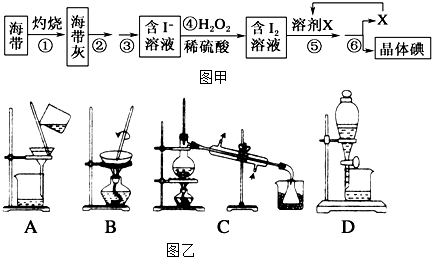

 ⑤
⑤ ⑥HOCH2CH2CH2COOH
⑥HOCH2CH2CH2COOH