题目内容
家用炒菜铁锅用水清洗放置后出现红棕色的锈斑,在此变化过程中不发生的化学反应是( )
| A、4Fe(OH)2+2H2O+O2=4Fe(OH)3↓ |
| B、2Fe+2H2O+O2=2Fe(OH)2↓ |
| C、2H2O+O2+4e-=4OH- |
| D、Fe-3e-=Fe3+ |
考点:金属的电化学腐蚀与防护,铁的氧化物和氢氧化物
专题:电化学专题
分析:烧过菜的铁锅未及时洗涤(残液中含NaCl等),第二天便出现红棕色锈斑[Fe(OH)3失水的产物],是金属铁发生吸氧腐蚀的结果,正极发生的是氧气得电子的还原反应,负极是金属铁是失电子的氧化反应.
解答:
解:A、氢氧化亚铁不稳定,易被氧气氧化为氢氧化铁,即4Fe(OH)2+O2+2H2O═4Fe(OH)3,故A不选;
B、正极发生的是氧气得电子的还原反应,即2H2O+O2+4e-═4OH-,负极是金属铁是失电子的氧化反应,即Fe-2e-═Fe2+,Fe2++2OH-═Fe(OH)2,合并得到:2Fe+2H2O+O2═2Fe(OH)2↓,故B不选;
C、金属铁发生吸氧腐蚀,正极发生的是氧气得电子的还原反应,即2H2O+O2+4e-═4OH-,故C不选;
D、金属铁发生吸氧腐蚀,负极是金属铁是失电子的氧化反应,即Fe-2e-═Fe2+,所以Fe-3e-=Fe3+不发生,故D选;
故选:D.
B、正极发生的是氧气得电子的还原反应,即2H2O+O2+4e-═4OH-,负极是金属铁是失电子的氧化反应,即Fe-2e-═Fe2+,Fe2++2OH-═Fe(OH)2,合并得到:2Fe+2H2O+O2═2Fe(OH)2↓,故B不选;
C、金属铁发生吸氧腐蚀,正极发生的是氧气得电子的还原反应,即2H2O+O2+4e-═4OH-,故C不选;
D、金属铁发生吸氧腐蚀,负极是金属铁是失电子的氧化反应,即Fe-2e-═Fe2+,所以Fe-3e-=Fe3+不发生,故D选;
故选:D.
点评:本题考查了金属吸氧腐蚀的原理,可以根据原电池知识来回答,难度不大.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
化学与生活密切相关.下列说法不正确的是( )
| A、氧化铁常用作红色油漆和涂料 |
| B、硅胶可作袋装食品的干燥剂 |
| C、二氧化硅是将太阳能转化为电能的常用材料 |
| D、氢氧化铝可作胃酸的中和剂 |
将常温下pH=12的氢氧化钠溶液与pH=2的硫酸溶液分别加热,溶液pH的变化是( )
| A、前者减少后者不变 |
| B、前者减小后者增大 |
| C、都不变 |
| D、都减小 |
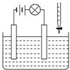 测定电解质溶液导电性的实验装置如图所示,向1mol?L-1氢氧化钡溶液中逐滴加入下列溶液,灯泡不是由亮→暗→亮的是( )
测定电解质溶液导电性的实验装置如图所示,向1mol?L-1氢氧化钡溶液中逐滴加入下列溶液,灯泡不是由亮→暗→亮的是( )| A、12 mol?L-1的浓盐酸 |
| B、硫酸铜溶液 |
| C、硫酸镁溶液 |
| D、稀硫酸 |
下列有关叙述中,错误的是( )
| A、肥皂的主要成分是油脂 |
| B、油脂是由高级脂肪酸和甘油所生成的酯 |
| C、酶也是一种蛋白质 |
| D、蛋白质的相对分子质量通常很大,有的甚至达到几万或几百万 |
下列反应的生成物为纯净物的是( )
| A、CH4与Cl2取代 |
| B、乙烯和氯化氢加成 |
| C、氯乙烯加聚 |
| D、丙烯和溴化氢加成 |
汶川大地震告诉人们应该懂得一 些在突发灾害时逃生、自救的手段.例如,当高层楼房下层起火,火势凶猛无法扑灭时,下列逃生措施中正确的是:①沿楼梯迅速下楼;②用湿毛巾堵住口鼻;③匍匐前进,寻找安全出口;④封闭房门;⑤迅速转移到阳台,用绳索下坠;⑥跳楼( )
| A、②③④⑤ | B、①②③④ |
| C、①②④⑤ | D、③④⑤⑥ |
BaCl2剧毒,致死量为0.3g,万一不慎误服,应按第7题的处理外,还应服用适量解毒剂,此解毒剂应是( )
| A、AgNO3 |
| B、CuSO4 |
| C、Na2CO3 |
| D、MgSO4 |