题目内容
4.两种气态烃的混合物共0.1mol,充分燃烧后得3.584L(标准状况下)CO2和3.6g水,下列说法正确的是( )| A. | 一定有甲烷 | B. | 一定有乙烯 | C. | 可能有乙烷 | D. | 一定有丙炔 |
分析 n(CO2)=$\frac{3.584L}{22.4L/mol}$=0.16mol,n(H2O)=$\frac{3.6g}{18g/mol}$=0.2mol,则混合的平均化学式为C1.6H4,因是混合物,则肯定含有C原子数小于1.6的烃,即一定含有甲烷,因甲烷中含有4个氢原子,则另一种烃也含有4个氢原子,以此解答该题.
解答 解:两种气态烃的混合物共0.1mol,充分燃烧后得3.58L(标准状况下)CO2和3.6g水,
则:n(CO2)=$\frac{3.584L}{22.4L/mol}$=0.16mol,n(H2O)=$\frac{3.6g}{18g/mol}$=0.2mol,
则混合的平均化学式为C1.6H4,因是混合物,则肯定含有C原子数小于1.6的烃,即一定含有甲烷,
因甲烷中含有4个氢原子,则另一种烃也含有4个氢原子,乙烷中H原子数目大于4,不可能含有,可能含有乙烯、丙炔等,
故选A.
点评 本题考查分子式的确定、混合物计算,题目难度中等,利用平均分子组成判断烃的组成为解答关键,试题侧重考查学生的分析能力及灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.直接提供电能的反应一般是放热反应,下列反应中能提供电能的是( )
| A. | Ba(OH)2•8H2O与NH4Cl反应 | B. | 酸碱中和反应 | ||
| C. | 灼热的炭与CO2反应 | D. | H2与Cl2燃烧反应 |
15.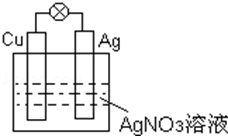 如图所示的原电池中:
如图所示的原电池中:
①导线中电子的流向Cu→Ag,
②溶液中阳离子的移动方向向银电极移动,
③正极的电极反应式为Ag++e-=Ag,
④电池工作时总反应的离子方程式是Cu+2Ag+═2Ag+Cu2+.
 如图所示的原电池中:
如图所示的原电池中:①导线中电子的流向Cu→Ag,
②溶液中阳离子的移动方向向银电极移动,
③正极的电极反应式为Ag++e-=Ag,
④电池工作时总反应的离子方程式是Cu+2Ag+═2Ag+Cu2+.
12.未来新能源的特点是资源丰富,在使用时对环境无污染或污染很小,且可以再生.下列属于未来新能源标准的是( )
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能.
①天然气 ②煤 ③核能 ④石油 ⑤太阳能 ⑥生物质能 ⑦风能 ⑧氢能.
| A. | ①②③④ | B. | ⑤⑥⑦⑧ | C. | ①③⑤⑥⑦⑧ | D. | ③④⑤⑥⑦⑧ |
19.下列物质不能跟铝反应并生成氢气的是( )
| A. | 甲酸溶液 | B. | 氢氧化钠溶液 | C. | 氯化铵溶液 | D. | 硫酸钠溶液 |
16.下列各组物质,可以直接用分液漏斗分离的是( )
| A. | 酒精和碘 | B. | 硝基苯和水 | C. | 乙醇和水 | D. | 溴和溴苯 |
13.实验室用足量锌粒与一定量的2mol/L硫酸溶液反应制取氢气,下列措施既能减小化学反应速率,又不影响氢气产量的选项是( )
| A. | 用锌粒代替锌粉 | B. | 向其中加入少量1mol/L硫酸溶液 | ||
| C. | 向其中加入氯化钠溶液 | D. | 向其中加入等体积的水 | ||
| E. | 向其中加入碳酸钠溶液 | F. | 向其中加入硝酸钠溶液 |
14.有关NaHCO3和Na2CO3的性质,以下叙述错误的是( )
| A. | 等质量的NaHCO3和Na2CO3与足量盐酸反应,在相同条件下NaHCO3产生的CO2体积大 | |
| B. | 等物质的量的两种盐与同浓度盐酸完全反应,所消耗盐酸的体积Na2CO3是NaHCO3的两倍 | |
| C. | 将石灰水加入NaHCO3溶液中无沉淀,加入Na2CO3溶液中有白色沉淀 | |
| D. | 等浓度的两种盐溶液分别与等浓度的盐酸反应,碳酸氢钠溶液的反应速率快 |