题目内容
12.反应2A(g)+B(g)?3C(g),起始时按5:2的体积比把A,B两气体混合后,充入一体积不变的密闭容器中,在恒定温度下使其反应,达平衡时混合气体中C的体积分数为60%.(1)A的转化率为56%,B的转化率为70%;
(2)平衡时压强与起始时压强之比为1:1.
分析 起始时按5:2的体积比把A、B两气体混合后,相同条件下,气体的体积之比等于物质的量之比,设A、B的物质的量分别为5n、2n,转化的B为x,则
2A(g)+B(g)?3C(g)
开始 5n 2n 0
转化 2x x 3x
平衡 5n-2x 2n-x 3x
达平衡时混合气体中C的体积分数为60%,则
$\frac{3x}{5n-2x+2n-x+3x}$×100%=60%,
解得x=1.4n,
结合转化率=$\frac{转化的量}{开始的量}$、压强之比等于物质的量之比计算.
解答 解:起始时按5:2的体积比把A、B两气体混合后,相同条件下,气体的体积之比等于物质的量之比,设A、B的物质的量分别为5n、2n,转化的B为x,则
2A(g)+B(g)?3C(g)
开始 5n 2n 0
转化 2x x 3x
平衡 5n-2x 2n-x 3x
达平衡时混合气体中C的体积分数为60%,则
$\frac{3x}{5n-2x+2n-x+3x}$×100%=60%,
解得x=1.4n,
(1)A的转化率为$\frac{2×1.4n}{5n}$×100%=56%,B的转化率为$\frac{1.4n}{2n}$×100%=70%,
故答案为:56%;70%;
(2)相同条件下,压强之比等于物质的量之比,则平衡时压强与起始时压强之比为$\frac{5n-2x+2n-x+3x}{5n+2n}$=1:1,故答案为:1:1.
点评 本题考查化学平衡的计算,为高频考点,把握化学平衡三段法、转化率计算为解答的关键,侧重分析与计算能力的考查,注意物质的量与压强、体积的关系,题目难度不大.

 步步高达标卷系列答案
步步高达标卷系列答案| A. | 元素B的化合物可以用来做焰火材料 | |
| B. | 化合物AE与CE含有相同类型的化学键 | |
| C. | 工业上常用电解法制备元素C、D、E的单质 | |
| D. | 元素B、D的最高价氧化物对应的水化物之间可能发生反应 |
| A. | NO2 | B. | NO | C. | H2 | D. | Cl2 |
| A. |  闻氯气的气味 | B. | 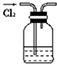 用排饱和食盐水法收集氯气 | ||
| C. |  盛装液氯的容器 | D. | 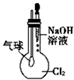 证明氯气可以与NaOH溶液反应 |
| A. | 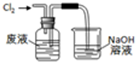 氧化废液中的溴化氢 | B. |  分离CCl4层和水层 | ||
| C. | 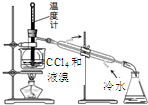 分离四氯化碳和液溴 | D. | 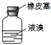 储存液溴 |


 上四 个碳原子各连接1个支链或取代基.
上四 个碳原子各连接1个支链或取代基.