题目内容
如图表示NH4NO3和D物质为初始反应物发生的一系列变化,其中,在常温下B为液态,F为不溶于水但可溶于酸的白色固体,G与I为无色气体,G能使湿润的红色石蕊试纸变蓝.

(1)D和H的化学式:D ,H ,G与E的电子式:G ,E .
(2)写出下列反应的方程式:反应① ;反应② .

(1)D和H的化学式:D
(2)写出下列反应的方程式:反应①
考点:无机物的推断
专题:推断题
分析:由转化关系可知硝酸分解生成的A为HNO3,B为H2O,G能使湿润的红色石蕊试纸变蓝,应为NH3,F为不溶于水但可溶于酸的白色固体,则可知E和B的反应为Mg3N2和水的反应,F为Mg(OH)2,D为Mg,H为Mg(NO3)2,I为H2,结合对应物质的性质解答该题.
解答:
解:由转化关系可知硝酸分解生成的A为HNO3,B为H2O,G能使湿润的红色石蕊试纸变蓝,应为NH3,F为不溶于水但可溶于酸的白色固体,则可知E和B的反应为Mg3N2和水的反应,F为Mg(OH)2,D为Mg,H为Mg(NO3)2,I为H2,E为Mg3N2,电子式为Mg2+ Mg2+
Mg2+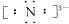 Mg2+;,
Mg2+;,
(1)由以上分析可知,D为Mg,H为Mg(NO3)2,G为NH3,电子式为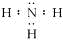 ,
,
故答案为:Mg;Mg(NO3)2;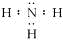 ;Mg2+
;Mg2+ Mg2+
Mg2+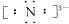 Mg2+;
Mg2+;
(2)①反应①的方程式为5NH4NO3
2HNO3+4N2↑+9H2O,故答案为:5NH4NO3
2HNO3+4N2↑+9H2O;
②反应②的方程式为3Mg+N2
Mg3N2,故答案为:3Mg+N2
Mg3N2
 Mg2+
Mg2+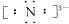 Mg2+;,
Mg2+;,(1)由以上分析可知,D为Mg,H为Mg(NO3)2,G为NH3,电子式为
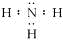 ,
,故答案为:Mg;Mg(NO3)2;
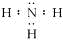 ;Mg2+
;Mg2+ Mg2+
Mg2+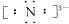 Mg2+;
Mg2+;(2)①反应①的方程式为5NH4NO3
| ||
| ||
②反应②的方程式为3Mg+N2
| ||
| ||
点评:本题考查无机物的推断,为高频考点,侧重于学生的分析能力的考查,注意把握物质的性质,本题突破口为硝酸的分解以及氨气的性质,难度中等.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
X、Y是周期表中前20号中两种元素(非稀有气体元素),X原子的半径比Y的半径小,且具有相同的电子层数,下列有关叙述正确的是(选项中m、n均为正整数)( )
| A、若Y最高价为+5,则X最高价一定为+6或+7 |
| B、若Y元素形成的单质是气体,则X元素形成的单质一定也是气体 |
| C、若HnXOm为强酸,则X的氢化物溶液于水一定显酸性 |
| D、X的离子半径一定比Y离子半径小 |
 已知2SO2(g)+O2(g)
已知2SO2(g)+O2(g)