题目内容
下列各组物质中,酸性由强到弱排列顺序错误的是( )
| A、HClO4 H2SO4 H3PO4 |
| B、HClO4 HClO3 HClO2 |
| C、HClO HBrO4 HIO4 |
| D、H2SO4 H2SO3 H2CO3 |
考点:非金属在元素周期表中的位置及其性质递变的规律
专题:元素周期律与元素周期表专题
分析:非金属元素的最高价含氧酸中,元素的非金属性越强其最高价含氧酸的酸性越强;对于同一种元素的含氧酸来说,该元素的化合价越高,其含氧酸的酸性越强.
解答:
解:A.P、S、Cl元素处于同一周期,且非金属性逐渐增强,且这几种酸都是其相应的最高价含氧酸,所以HClO4 H2SO4 H3PO4酸性逐渐减弱,故A不选;
B.这几种酸都是氯元素的不同含氧酸,氯元素的化合价越高其酸性越强,所以HClO4 H2SO4 H3PO4的酸性逐渐减弱,故B不选;
C.高溴酸的酸性比高碘酸强,且高溴酸和高碘酸都是强酸,次氯酸是弱酸,所以酸性由强到弱的顺序是HBrO4 HIO4 HClO,故C选;
D.硫酸的酸性比亚硫酸强,亚硫酸的酸性比碳酸的强,所以这几种酸的酸性逐渐减弱,故D不选;
故选C.
B.这几种酸都是氯元素的不同含氧酸,氯元素的化合价越高其酸性越强,所以HClO4 H2SO4 H3PO4的酸性逐渐减弱,故B不选;
C.高溴酸的酸性比高碘酸强,且高溴酸和高碘酸都是强酸,次氯酸是弱酸,所以酸性由强到弱的顺序是HBrO4 HIO4 HClO,故C选;
D.硫酸的酸性比亚硫酸强,亚硫酸的酸性比碳酸的强,所以这几种酸的酸性逐渐减弱,故D不选;
故选C.
点评:本题考查酸性强弱的比较,注意非金属的非金属性强弱决定其最高价含氧酸的酸性强弱,但不决定其低价含氧酸的酸性强弱,为易错点,题目难度不大.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
已知酸性强弱顺序为H2CO3>C6H5OH>HCO3-,下列化学方程式正确的是( )
| A、C6H5ONa+H2O+CO2→C6H5OH+Na2CO3 |
| B、C6H5OH+NaHCO3→C6H5ONa+H2O+CO2↑ |
| C、C6H5OH+Na2CO3→C6H5ONa+H2O+CO2↑ |
| D、C6H5OH+Na2CO3→C6H5ONa+NaHCO3 |
物质的量相同的下列各物质分别在足量的O2中完全燃烧,其中耗氧量相同的一组是( )
| A、CH3OH 和C3H6 |
| B、C3H7COOH 和C2H5COCH3 |
| C、C2H5CHO 和C3H4 |
| D、C3H8 和C4H4 |
用价层电子对互斥理论预测NH3和BF3的空间构型,结论正确的是( )
| A、直线形;三角锥形 |
| B、V形;三角锥形 |
| C、三角锥形;平面三角形 |
| D、直线形;平面三角形 |
下列说法中错误的是( )
| A、当中心原子的配位数为6时,物质常呈八面体空间结构 |
| B、[Ag(NH3)2]+中Ag+提供空轨道 |
| C、配位数为4的配合物均为正四面体结构 |
| D、已知[Cu(NH3)2]2+的中心原子采用sp杂化,则它们的空间构型为直线型 |
下列各物质中,不属于同分异构体的是( )
A、丙烯与 |
B、 |
C、 |
D、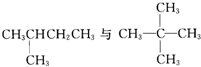 |
在元素周期表短周期中的X和Y两种元素可组成化合物XY3,下列说法正确的是( )
| A、XY3一定是共价化合物 |
| B、若Y的原子序数为n,X的原子序数一定是n±4 |
| C、X和Y可属于同一周期,也可属于两个不同的周期 |
| D、X和Y一定不属于同一主族 |
关于氢键,下列说法正确的是( )
| A、每一个水分子内含有两个氢键 |
| B、冰、水和水蒸气中都存在氢键 |
| C、HF的沸点比HI高,是由于HF分子间存在氢键所致 |
| D、H2O是一种非常稳定的化合物这是由于氢键所致 |
不能使酸性KMnO4溶液褪色的是( )
| A、乙烯 | B、乙苯 | C、乙烷 | D、乙炔 |