题目内容
3.下列反应属于取代反应的是( )| A. | 由乙烯制取氯乙烷 | B. | 乙烷在空气中燃烧 | ||
| C. | 乙烷在光照下与氯气反应 | D. | 乙烯使酸性高锰酸钾溶液褪色 |
分析 A.碳碳双键转化为单键;
B.燃烧为氧化反应;
C.乙烷中H被Cl取代;
D.乙烯含碳碳双键,能被高锰酸钾氧化.
解答 解:A.由乙烯制取氯乙烷,为加成反应,故A不选;
B.乙烷在空气中燃烧,为氧化反应,故B不选;
C.乙烷在光照下与氯气反应,为取代反应,故C选;
D.乙烯使酸性高锰酸钾溶液褪色,为氧化反应,故D不选;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应为解答的关键,侧重分析与应用能力的考查,注意有机物的反应条件,题目难度不大.

练习册系列答案
相关题目
13.有下列几种方法制备O2:(1)KClO3和MnO2共热,(2)H2O2中加MnO2,(3)KMnO4受热分解,若要制相同质量的O2,则上述反应中相关物质转移的电子数之比为( )
| A. | 3:2:4 | B. | 1:1:1 | C. | 2:1:2 | D. | 1:2:1 |
14.常温下将pH=9的Ba(OH)2溶液稀释500倍,稀释溶液后,c (OH-)与c (Ba2+)的比值近似为( )
| A. | 1:1 | B. | 1:2 | C. | 10:1 | D. | 2:1 |
18.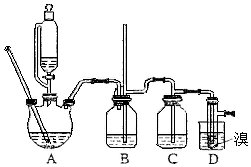 实验室制备1,2-二溴乙烷,用16.0g的溴和足量的乙醇制备1,2-二溴乙烷,实验结束后得到9.4g产品.实验装置如图所示:
实验室制备1,2-二溴乙烷,用16.0g的溴和足量的乙醇制备1,2-二溴乙烷,实验结束后得到9.4g产品.实验装置如图所示:
有关数据列表:
请回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其主要目的是d(填正确选项前的字母;
a、引发反应 b、加快反应速度 c、防止乙醇挥发 d、减少副产物乙醚生成
(2)在装置C中应加入c,其目的是吸收乙烯中的酸性杂质气体;(填正确选项前的字母)
a、水 b、浓硫酸 c、氢氧化钠溶液 d、酸性KMnO4溶液
(3)判断该制备反应已经结束的最简单的方法是溴的颜色完全褪去.
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”或“下”);
(5)在装置B中较长玻璃导管的作用是防止倒吸、判断装置是否堵塞;
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发,但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞;
(7)本实验中,1,2-二溴乙烷的产率为50%.
 实验室制备1,2-二溴乙烷,用16.0g的溴和足量的乙醇制备1,2-二溴乙烷,实验结束后得到9.4g产品.实验装置如图所示:
实验室制备1,2-二溴乙烷,用16.0g的溴和足量的乙醇制备1,2-二溴乙烷,实验结束后得到9.4g产品.实验装置如图所示:有关数据列表:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/0C | 78.5 | 132 | 34.6 |
| 熔点/0C | -130 | 9 | -116 |
| 溶解性 | 易溶水 | 难溶水 | 微溶于水 |
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其主要目的是d(填正确选项前的字母;
a、引发反应 b、加快反应速度 c、防止乙醇挥发 d、减少副产物乙醚生成
(2)在装置C中应加入c,其目的是吸收乙烯中的酸性杂质气体;(填正确选项前的字母)
a、水 b、浓硫酸 c、氢氧化钠溶液 d、酸性KMnO4溶液
(3)判断该制备反应已经结束的最简单的方法是溴的颜色完全褪去.
(4)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”或“下”);
(5)在装置B中较长玻璃导管的作用是防止倒吸、判断装置是否堵塞;
(6)反应过程中应用冷水冷却装置D,其主要目的是乙烯与溴反应时放热,冷却可避免溴的大量挥发,但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的凝固点较低(9℃),过度冷却会使其凝固而使气路堵塞;
(7)本实验中,1,2-二溴乙烷的产率为50%.
8. (1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1;反应Fe(s)+H2O(g)?FeO(s)+H2(g)△H2,平衡常数为K2.在不同温度时K1、K2的值如表:
(1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1;反应Fe(s)+H2O(g)?FeO(s)+H2(g)△H2,平衡常数为K2.在不同温度时K1、K2的值如表:
①反应 CO2(g)+H2(g)?CO(g)+H2O(g)△H,平衡常数K,则△H=△H1-△H2(用△H1和△H2表示),K=$\frac{{K}_{1}}{{K}_{2}}$(用K1和K2表示),且由上述计算可知,反应CO2(g)+H2(g)?CO(g)+H2O(g)是吸热反应(填“吸热”或“放热”).
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H>0,CO2的浓度与时间的关系如图所示:
①该条件下反应的平衡常数为2.0;
②下列措施中能使平衡时$\frac{c(CO)}{c(C{O}_{2})}$增大的是A(填序号)
A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
③一定温度下,在一个固定容积的密闭容器中发生上述反应,下列能判断该反应达到化学平衡状态的是bc(填字母).
a.容器中压强不变 b.气体的密度不再改变c.v正(CO2)=v逆(CO) d.c(CO2)=c(CO) e.容器内气体总物质的量不变.
 (1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1;反应Fe(s)+H2O(g)?FeO(s)+H2(g)△H2,平衡常数为K2.在不同温度时K1、K2的值如表:
(1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1;反应Fe(s)+H2O(g)?FeO(s)+H2(g)△H2,平衡常数为K2.在不同温度时K1、K2的值如表:| 700℃ | 900℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H>0,CO2的浓度与时间的关系如图所示:
①该条件下反应的平衡常数为2.0;
②下列措施中能使平衡时$\frac{c(CO)}{c(C{O}_{2})}$增大的是A(填序号)
A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
③一定温度下,在一个固定容积的密闭容器中发生上述反应,下列能判断该反应达到化学平衡状态的是bc(填字母).
a.容器中压强不变 b.气体的密度不再改变c.v正(CO2)=v逆(CO) d.c(CO2)=c(CO) e.容器内气体总物质的量不变.
15.下列有关说法正确的是( )
| A. | HClO是弱酸,但NaClO强电解质 | |
| B. | HC1、SO2、HBr三种气体都可用浓硫酸干燥 | |
| C. | 向浓氨水中滴加FeCl3饱和溶液,可制得Fe(OH)3胶体 | |
| D. | SO2和SO3都是酸性氧化物,两者的水溶液都是二元强酸 |
12.下列有关说法正确的是( )
| A. | 0.1L物质的量浓度为2mol/L的(NH4)2S溶液中含有的S2-数目为0.2×6.02×1023 | |
| B. | 对NaCl溶液和金属钠加热,都会使导电能力增强 | |
| C. | 25℃时,向0.1mol/LCH3COOH溶液中加入少量CH3COONa固体,该溶液中水的电离程度将增大,且Kw不变 | |
| D. | 用惰性电极电解1L 1mol/L的CuSO4溶液,当阴极析出3.2g铜时,加入0.05mol Cu(OH)2固体可将溶液浓度恢复至元浓度 |
7.第21届联合国气候大会于2015年11月30日在巴黎召开,会议的主题是减少温室气体排放量.
Ⅰ.CO2加氢合成甲醇是合理利用 CO2的有效途径.由 CO2制备甲醇过程可能涉及反应如下:
反应①:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1=-49.58kJ•mol-1
反应②:CO2(g)+H2(g)?CO (g)+H2O(g)△H2
反应③:CO(g)+2H2(g)?CH3OH(g)△H3=-90.77kJ•mol-1,回答下列问题:
(1)反应②的△H2=+41.19 kJ•mol-1,反应 ①自发进行条件是较低温(填“较低温”、“较高温”或“任何温度”).
(2)某温度下,在体积为2L的恒容密闭容器中,按如下方式加入反应物,仅发生反应①.一段时间后达到平衡.
测得甲中CO2和CH3OH(g)的浓度随时间变化如图所示.
①前3min内,平均反应速率v(H2)=0.5mol•L-1•min-1.此温度下该反应的平衡常数为
5.33(结果保留两位小数).
②下列措施中,既能使反应速率加快,又能使n(CH3OH)/n(CO2)增大是D.
A.升高温度 B.充入惰性气体 C.将H2O(g)从体系中分离
D.再充入1mol H2 E.再充入1mol CO2 F.加入催化剂
③反应达到平衡后,若向反应体系再加入CO2(g)、H2(g)、CH3OH(g)、H2O(g)各1mol,化学平衡正向(填“正向”、“逆向”或“不”)移动.
④要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为1.5 mol/L<c≤2 mol/L.
Ⅱ.工业上可用CO2与NH3合成制尿素的原料氨基甲酸铵(H2NCOONH4).氨基甲酸铵极易发生:H2NCOONH4+2H2O?NH4HCO3+NH3•H2O,该反应酸性条件下更彻底.25℃,向l L 0.1mol•L-1的盐酸中逐渐加入氨基甲酸铵粉末至溶液呈中性(忽略溶液体积变化),共用去0.052mol氨基甲酸铵.若此时溶液中几乎不含碳元素,则该溶液中 c(NH4+)=0.1mol/L,NH4+水解常数Kh=4×10-9mol/L.
Ⅰ.CO2加氢合成甲醇是合理利用 CO2的有效途径.由 CO2制备甲醇过程可能涉及反应如下:
反应①:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H1=-49.58kJ•mol-1
反应②:CO2(g)+H2(g)?CO (g)+H2O(g)△H2
反应③:CO(g)+2H2(g)?CH3OH(g)△H3=-90.77kJ•mol-1,回答下列问题:
(1)反应②的△H2=+41.19 kJ•mol-1,反应 ①自发进行条件是较低温(填“较低温”、“较高温”或“任何温度”).
(2)某温度下,在体积为2L的恒容密闭容器中,按如下方式加入反应物,仅发生反应①.一段时间后达到平衡.
| 容器 | 甲 | 乙 |
| 反应物投入量 | 2mol CO2、6mol H2 | a mol CO2、b mol H2 c mol CH3OH(g)、c mol H2O(g) |

①前3min内,平均反应速率v(H2)=0.5mol•L-1•min-1.此温度下该反应的平衡常数为
5.33(结果保留两位小数).
②下列措施中,既能使反应速率加快,又能使n(CH3OH)/n(CO2)增大是D.
A.升高温度 B.充入惰性气体 C.将H2O(g)从体系中分离
D.再充入1mol H2 E.再充入1mol CO2 F.加入催化剂
③反应达到平衡后,若向反应体系再加入CO2(g)、H2(g)、CH3OH(g)、H2O(g)各1mol,化学平衡正向(填“正向”、“逆向”或“不”)移动.
④要使平衡后乙与甲中相同组分的体积分数相等,且起始时维持化学反应向逆反应方向进行,则c的取值范围为1.5 mol/L<c≤2 mol/L.
Ⅱ.工业上可用CO2与NH3合成制尿素的原料氨基甲酸铵(H2NCOONH4).氨基甲酸铵极易发生:H2NCOONH4+2H2O?NH4HCO3+NH3•H2O,该反应酸性条件下更彻底.25℃,向l L 0.1mol•L-1的盐酸中逐渐加入氨基甲酸铵粉末至溶液呈中性(忽略溶液体积变化),共用去0.052mol氨基甲酸铵.若此时溶液中几乎不含碳元素,则该溶液中 c(NH4+)=0.1mol/L,NH4+水解常数Kh=4×10-9mol/L.