题目内容
高纯度氧化铝有广泛的用途,某研究小组研究用以下流程制取高纯度氧化铝:
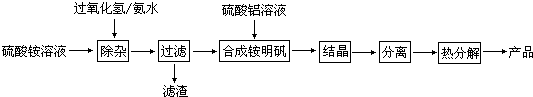
根据上述流程图填空:
(1)“除杂”操作是加入过氧化氢后,用氨水调节溶液的pH约为8.0,以除去硫酸铵溶液中的少量Fe2+.请写出在除去Fe2+离子的过程中,发生的主要反应的离子方程式 .
(2)通常条件下Ksp〔Fe(OH)3〕=4.0×10-38,除杂后溶液中c(Fe3+)约为 .
(3)配制硫酸铝溶液时,需用硫酸酸化,酸化的目的是 .
(4)“结晶”这步操作中,母液经蒸发浓缩至溶液表面刚出现薄层晶体即停止加热,然后冷却结晶,得到铵明矾晶体(含结晶水).母液不能蒸干的原因是 .
(5)“分离”操作的名称是 (填字母代号).A.蒸馏 B.分液 C.过滤
(6)铵明矾晶体的化学式为NH4Al(SO4)2?12H2O,在0.1mol/L铵明矾的水溶液中,离子浓度最大的离子是 ,离子浓度最小的离子是 .

根据上述流程图填空:
(1)“除杂”操作是加入过氧化氢后,用氨水调节溶液的pH约为8.0,以除去硫酸铵溶液中的少量Fe2+.请写出在除去Fe2+离子的过程中,发生的主要反应的离子方程式
(2)通常条件下Ksp〔Fe(OH)3〕=4.0×10-38,除杂后溶液中c(Fe3+)约为
(3)配制硫酸铝溶液时,需用硫酸酸化,酸化的目的是
(4)“结晶”这步操作中,母液经蒸发浓缩至溶液表面刚出现薄层晶体即停止加热,然后冷却结晶,得到铵明矾晶体(含结晶水).母液不能蒸干的原因是
(5)“分离”操作的名称是
(6)铵明矾晶体的化学式为NH4Al(SO4)2?12H2O,在0.1mol/L铵明矾的水溶液中,离子浓度最大的离子是
考点:金属的回收与环境、资源保护
专题:实验设计题
分析:(1)H2O2溶液具有强氧化性,可以氧化亚铁离子生成铁离子,铁离子在氨水存在的条件下生成氢氧化铁红褐色沉淀;
(2)根据氢氧化铁的溶度积及PH=8计算出铁离子浓度;
(3)铝离子在溶液中能够发生水解生成氢氧化铝;
(4)蒸干会析出可溶性杂质的析出,且Al3+水解程度增大;
(5)将晶体与溶液分离的操作是过滤;
(6)根据题中所给的化学式,利用铵根和铝离子水解进行解答即可.
(2)根据氢氧化铁的溶度积及PH=8计算出铁离子浓度;
(3)铝离子在溶液中能够发生水解生成氢氧化铝;
(4)蒸干会析出可溶性杂质的析出,且Al3+水解程度增大;
(5)将晶体与溶液分离的操作是过滤;
(6)根据题中所给的化学式,利用铵根和铝离子水解进行解答即可.
解答:
解:(1)检验Fe2+是否除尽的实验操作是:取少量除杂后的滤液,加适量H2O2溶液,振荡,滴加KSCN溶液,若无明显现象,说明Fe2+已除尽,
故答案为:取少量除杂后的滤液,加适量H2O2溶液,振荡,滴加KSCN溶液,若无明显现象,说明Fe2+已除尽;
(2)KSP[Fe(OH)3]=4.0×10-38,PH=8,溶液中氢氧根离子浓度为:1×10-6mol/L,c(Fe3+)=
mol/L=4.0×10-20mol/L,
故答案为:4.0×10-20mol/L;
(3)由于铝离子在溶液中能够发生水解生成氢氧化铝,所以加入硫酸酸化,抑制了铝离子的水解,故答案为:抑制Al3+水解;
(4)由于蒸干会析出可溶性杂质的析出,且Al3+水解程度增大,所以母液不能蒸干,故答案为:减少可溶性杂质的析出及Al3+水解;
(5)通过过滤,将硫酸铝晶体从溶液中分离,所以C正确;
故选C;
(6)铵明矾晶体的化学式为NH4Al(SO4)2?12H2O,在0.1mol/L铵明矾的水溶液中,未水解前,c(Al3+)=c(NH4+)=0.1mol/L,由于铵根和铝离子均水解,水解结合水电离出的氢氧根,故水解后浓度均小于0.1mol/L,c(SO42-)=0.2mol/L,0.2>0.1,故答案为:SO42-;OH-.
故答案为:取少量除杂后的滤液,加适量H2O2溶液,振荡,滴加KSCN溶液,若无明显现象,说明Fe2+已除尽;
(2)KSP[Fe(OH)3]=4.0×10-38,PH=8,溶液中氢氧根离子浓度为:1×10-6mol/L,c(Fe3+)=
| 4.0×10-38 |
| (1×10-6)3 |
故答案为:4.0×10-20mol/L;
(3)由于铝离子在溶液中能够发生水解生成氢氧化铝,所以加入硫酸酸化,抑制了铝离子的水解,故答案为:抑制Al3+水解;
(4)由于蒸干会析出可溶性杂质的析出,且Al3+水解程度增大,所以母液不能蒸干,故答案为:减少可溶性杂质的析出及Al3+水解;
(5)通过过滤,将硫酸铝晶体从溶液中分离,所以C正确;
故选C;
(6)铵明矾晶体的化学式为NH4Al(SO4)2?12H2O,在0.1mol/L铵明矾的水溶液中,未水解前,c(Al3+)=c(NH4+)=0.1mol/L,由于铵根和铝离子均水解,水解结合水电离出的氢氧根,故水解后浓度均小于0.1mol/L,c(SO42-)=0.2mol/L,0.2>0.1,故答案为:SO42-;OH-.
点评:本题考查工艺流程、离子检验、盐类水解、对条件的控制选择、物质的分离提纯等,理解工艺流程原理是解题的关键,是对学生综合能力的考查,需要学生具备扎实的基础与灵活运用能力,题目难度中等.

练习册系列答案
相关题目
下列叙述中正确的是( )
| A、1molNH3所含有的原子数为NA |
| B、常温常压下,22.4L氧气所含的原子数为2NA |
| C、常温常压下,48gO3所含的氧原子数为3NA |
| D、标准状况下,33.6LH2O含有9.03×1023个H2O分子 |
下列叙述正确的是( )
| A、金属氧化物一定是碱性氧化物 |
| B、非金属氧化物一定是酸性氧化物 |
| C、只有在标准状况下,气体的摩尔体积才能为22.4L/mol |
| D、非电解质在水溶液中和熔融状态下均以分子形式存在,因而不能导电 |
下列说法不正确的是( )
| A、检验食盐中含有钠离子,可以用焰色反应实验,如果焰色呈黄色则可以说明含有钠离子 |
| B、检验食盐中含有氯离子,则可以加用硝酸酸化的硝酸银溶液 |
| C、向溴水中加入食盐溶液,可以使溴水褪色 |
| D、食盐中加碘的作用是预防“大脖子病”的发生 |