题目内容
某物质分子结构式为 ,下列说法不正确的是( )
,下列说法不正确的是( )
 ,下列说法不正确的是( )
,下列说法不正确的是( )分析:A.同种元素之间形成非极性共价键,不同元素之间形成极性共价键;
B.分子中正负电荷中心不重合,从整个分子来看,电荷的分布是不均匀的,不对称的,这样的分子为极性分子,以极性键结合的双原子一定为极性分子,以极性键结合的多原子分子如结构对称,正负电荷的重心重合,电荷分布均匀,则为非极性分子;
C.C-Cl键和C-H键的键长不同;
D.卤代烃都不溶于水.
B.分子中正负电荷中心不重合,从整个分子来看,电荷的分布是不均匀的,不对称的,这样的分子为极性分子,以极性键结合的双原子一定为极性分子,以极性键结合的多原子分子如结构对称,正负电荷的重心重合,电荷分布均匀,则为非极性分子;
C.C-Cl键和C-H键的键长不同;
D.卤代烃都不溶于水.
解答:解:A.该分子为氯乙烯,其中C-Cl键和C-H键 属于极性共价键,C=C键属于非极性共价键,故A正确;
B.该分子结构不对称,属于极性分子,故B正确;
C.该分子相当于一个Cl原子取代乙烯分子中的一个H原子后得到的产物,所有的原子都处于同一个平面上,但是C-Cl键和C-H键的键长不同,所以其结构不再是平面正三角形,键角不再是120°,故C错误;
D.卤代烃都不溶于水,故D正确.
故选C.
B.该分子结构不对称,属于极性分子,故B正确;
C.该分子相当于一个Cl原子取代乙烯分子中的一个H原子后得到的产物,所有的原子都处于同一个平面上,但是C-Cl键和C-H键的键长不同,所以其结构不再是平面正三角形,键角不再是120°,故C错误;
D.卤代烃都不溶于水,故D正确.
故选C.
点评:本题考查键的极性和分子极性的判断,注意分子立体构型的判断,题目难度不大.

练习册系列答案
相关题目
 ,1mol该有机物在加热条件下与足量的NaOH溶液反应,最多可消耗NaOH的物质的量为3mol
,1mol该有机物在加热条件下与足量的NaOH溶液反应,最多可消耗NaOH的物质的量为3mol ,六个原子位于同一平面,键角为120°,下列说法不正确的是
,六个原子位于同一平面,键角为120°,下列说法不正确的是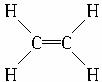 ,六个原子位于同一平面,键角为120°,下列说法不正确的是( )?
,六个原子位于同一平面,键角为120°,下列说法不正确的是( )?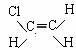 ,下列说法不正确的是( )
,下列说法不正确的是( )