题目内容
已知:CH2(g)+H2O(g)=CO(g)+3H2(g)△H=+206.2kJ?mol-1
CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=-247.4kJ?mol-1
则CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为 .
CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=-247.4kJ?mol-1
则CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为
考点:用盖斯定律进行有关反应热的计算
专题:
分析:已知:①CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.2kJ?mol-1
②CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=-247.4kJ?mol-1
结合盖斯定律①×2-②得CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H.
②CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=-247.4kJ?mol-1
结合盖斯定律①×2-②得CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H.
解答:
解:①CH4(g)+H2O(g)=CO(g)+3H2(g)△H=+206.2kJ?mol-1
②CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=-247.4kJ?mol-1
结合盖斯定律①×2-②得到CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=+659.8kJ?mol-1,
故答案为:CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=+659.8kJ?mol-1.
②CH4(g)+CO2(g)=2CO(g)+2H2(g)△H=-247.4kJ?mol-1
结合盖斯定律①×2-②得到CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为:CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=+659.8kJ?mol-1,
故答案为:CH4(g)+2H2O(g)=CO2(g)+4H2(g)△H=+659.8kJ?mol-1.
点评:本题考查了盖斯定律计算和热化学方程式书写方法,掌握基础是关键,题目较简单.

练习册系列答案
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
下列关于有机物的描述正确的是( )
| A、葡萄糖和果糖互为同分异构体,淀粉和纤维素也互为同分异构体 |
| B、淀粉、油脂和蛋白质都能发生水解反应 |
| C、多糖、蛋白质、脂肪和聚丙烯都属于高分子化合物 |
| D、汽油、柴油和植物油都是碳氢化合物 |
在某容积一定的决斗容器中,有下列可逆反应2A(g)+B(g)?xC(g),反应曲线(T表示温度,P表示压强,C% 表示C的体积分数)如图所示,试判断对图的说法中正确的是( )
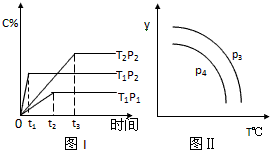

| A、x=2 |
| B、该反应是吸热反应 |
| C、P3>P4,y轴表示B的转化率 |
| D、P3<P4,y轴表示混合气体的密度 |
化学与生产生活、环境保护密切相关.下列说法中不正确的是( )
| A、食盐既可作调味品也可作食品防腐剂 |
| B、向海水中加入净水剂明矾可以使海水淡化 |
| C、加大石油、煤炭的开采速度,增加化石燃料的供应不利于“蓝天工程”的建设 |
| D、高铁车厢材料大部分采用铝合金,因为铝合金强度大、质量轻、抗腐蚀能力强 |
 全固态锂硫电池是一种新型电池,其能且密度约为一般电子设备中广泛使用的锂离子电池的4倍,且成本更低廉.已知锂硫电池的总反应为2Li+S
全固态锂硫电池是一种新型电池,其能且密度约为一般电子设备中广泛使用的锂离子电池的4倍,且成本更低廉.已知锂硫电池的总反应为2Li+S| 放电 |
| 充电 |
| A、乙池溶液中的N03一移向铁电极 |
| B、乙池石墨电极反应式为Ag++e-=Ag |
| C、甲池充电时,锂电极发生氧化反应 |
| D、甲池中消耗14g锂,乙池中产生11.2L氧气《标准状况下) |
NA为阿伏伽德罗常数,下列叙述正确的是( )
| A、18gH2O中含有的质子数为NA |
| B、常温常压下,Na2O2与足量H2O反应,每生成1 molO2,转移电子的数目为4NA |
| C、46gNO2和N2O4混合气体中含有原子总数为3NA |
| D、物质的量浓度为0.5 mol?L-1的MgCl2的溶液中,含有Cl-个数为NA |
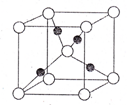 A、B、C、D、E为前四周期中原子序数依次增大的元素,相关的信息如下:
A、B、C、D、E为前四周期中原子序数依次增大的元素,相关的信息如下: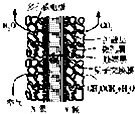 二甲醚(CH3OCH3)可作为洁净的液体化石燃料,以CO和H2为原料生产二甲醚的一种工艺主要发生以下三个反应:
二甲醚(CH3OCH3)可作为洁净的液体化石燃料,以CO和H2为原料生产二甲醚的一种工艺主要发生以下三个反应: