题目内容
 靛蓝是一种食品用合成色素,但对人体有害.使用时必须严格控制使用量.靛蓝允许小于0.1g?kg-1.靛蓝结构简式如图所示.下列关于靛蓝的叙述错误的是( )
靛蓝是一种食品用合成色素,但对人体有害.使用时必须严格控制使用量.靛蓝允许小于0.1g?kg-1.靛蓝结构简式如图所示.下列关于靛蓝的叙述错误的是( )| A、靛蓝可与溴水发生加成反应,使溴水褪色 |
| B、它的分子式是C16H10N2O2 |
| C、该物质分子量较大是高分子化合物 |
| D、它与氢气发生加成反应,1mol靛蓝需氢气最大量是9mol |
考点:有机物的结构和性质
专题:
分析:该有机物中含苯环、C=C、C=O,结合苯、烯烃、酮的性质来解答.
解答:
解:A.靛蓝中含有碳碳双键,可发生加成反应,故A正确;
B.由结构简式可知分子式是C16H10N2O2,故B正确;
C.有机物相对分子质量较小,不是高分子化合物,一般来说,高分子化合物的相对分子质量在10000以上,故C错误;
D.靛蓝中的碳碳双键、碳氧双键、苯环都可与氢气加成,1mol靛蓝需氢气最大量是9mol,故D正确.
故选C.
B.由结构简式可知分子式是C16H10N2O2,故B正确;
C.有机物相对分子质量较小,不是高分子化合物,一般来说,高分子化合物的相对分子质量在10000以上,故C错误;
D.靛蓝中的碳碳双键、碳氧双键、苯环都可与氢气加成,1mol靛蓝需氢气最大量是9mol,故D正确.
故选C.
点评:本题考查有机物的结构与性质,为高频考点,注意把握官能团与性质的关系,熟悉苯、烯烃的性质即可解答,题目难度不大.

练习册系列答案
相关题目
常温,向一定体积V mL浓度均为 0.1mol?L-1 FeCl3和FeCl2溶液中滴加NaOH溶液至pH=4,溶液中有沉淀生成,过滤,得到沉淀和滤液.已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Fe(OH)2]=8.0×10-16.下列说法正确的是( )
| A、滤液中c(Fe3+)=4.0×10-29mol?L-1 |
| B、沉淀为Fe(OH)3和Fe(OH)2的混合物 |
| C、向滤液中加入少量FeCl2溶液,一定有沉淀生成 |
| D、向滤液中继续加入NaOH溶液使pH>7时,有Fe(OH)2沉淀生成 |
下列说法不正确的是( )
| A、Ksp与温度有关 |
| B、由于Ksp(ZnS)>Ksp(CuS),所以ZnS沉淀在一定条件下可转化为CuS沉淀 |
| C、向AgCl沉淀的溶解平衡中加入NaCl固体,AgCl平衡不移动 |
| D、若在Ca(OH)2溶液与FeCl2溶液中加足量稀硝酸,无沉淀产生 |
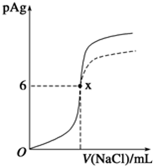 已知:pAg=-lg{c(Ag+)},Ksp(AgCl)=1×10-12.如图是向10mL AgNO3溶液中逐渐加入0.1mol?L-1的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).根据图象所得下列结论正确的是[提示:Ksp(AgCl)>Ksp(AgI)]( )
已知:pAg=-lg{c(Ag+)},Ksp(AgCl)=1×10-12.如图是向10mL AgNO3溶液中逐渐加入0.1mol?L-1的NaCl溶液时,溶液的pAg随着加入NaCl溶液的体积(单位mL)变化的图象(实线).根据图象所得下列结论正确的是[提示:Ksp(AgCl)>Ksp(AgI)]( )| A、原AgNO3溶液的物质的量浓度为1mol?L-1 |
| B、图中x点的坐标为(100,6) |
| C、若升高温度,图象不会发生变化 |
| D、把0.1mol?L-1的NaCl换成0.1mol?L-1 NaI则图象在终点后变为虚线部分 |
已知Ksp(Ag2CrO4)=9.0×10-12,将等体积的4×10-3mol?L-1的AgNO3溶液和4×10-3mol?L-1的K2CrO4溶液混合,下列说法正确的是( )
| A、恰好形成Ag2CrO4饱和溶液 |
| B、能析出Ag2CrO4沉淀 |
| C、不能析出Ag2CrO4沉淀 |
| D、无法确定能否析出Ag2CrO4沉淀 |
下列说法正确的是( )
| A、海南岛四面环海,水资源丰富,不必节约用水 |
| B、明矾既能沉降水中的悬浮物,又能杀菌消毒 |
| C、可通过长期饮用含Ca2+浓度较高的水来补钙 |
| D、若不慎接触敌敌畏或甲胺磷,最好用碱性肥皂液清洗 |
实验中需要2mol?L-1的Na2CO3溶液950mL,配制时,你认为应该选用的容量瓶的规格和称取的碳酸钠质量分别是( )
| A、1000 mL,212 g |
| B、950 mL,201.4 g |
| C、500 mL,286 g |
| D、任意规格,572 g |
