题目内容
钢铁企业酸洗钢材时产生的废液主要成分为Fe2+、H+、Cl-,可用下述方法处理该废液,回收盐酸和制备氧化铁涂料.

(1)单质X的化学式是 .
(2)氯化亚铁溶液经高温喷雾焙烧转化为HCl气体和氧化铁粉末,有关的化学方程式依次为: .
(3)某铁红涂料中除含有Fe2O3外,还可能添加有CuO或FeO中的一种,请设计实验方案,探究该铁红涂料中添加物的成分.
①提出合理假设
假设1:添加了CuO
假设2:添加了FeO
②请设计方案,验证上述假设,写出实验步骤、预期现象和结论.
限选试剂:铁粉、3mol?L-1 H2SO4、0.1mol?L-1酸性KMnO4溶液、10% NaOH溶液、10% H2O2、KSCN溶液
(4)请计算,用635g水完全吸收“高温喷雾焙烧”产生的HCl气体 升(标准状况),即可得到36.5%的浓盐酸(相对原子质量 Cl-35.5 H-1).

(1)单质X的化学式是
(2)氯化亚铁溶液经高温喷雾焙烧转化为HCl气体和氧化铁粉末,有关的化学方程式依次为:
(3)某铁红涂料中除含有Fe2O3外,还可能添加有CuO或FeO中的一种,请设计实验方案,探究该铁红涂料中添加物的成分.
①提出合理假设
假设1:添加了CuO
假设2:添加了FeO
②请设计方案,验证上述假设,写出实验步骤、预期现象和结论.
限选试剂:铁粉、3mol?L-1 H2SO4、0.1mol?L-1酸性KMnO4溶液、10% NaOH溶液、10% H2O2、KSCN溶液
| 操作步骤 | 预期现象和结论 |
| 步骤1.取少量样品于试管1中, | 样品全部溶解,得到澄清的溶液. |
| 步骤2. 步骤3. |
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:实验目的为盐酸和制备氧化铁涂料,则所加单质X应为Fe,可与盐酸反应生成FeCl2,过滤后将滤液高温焙烧,转化为HCl气体和氧化铁粉末,涉及反应为FeCl2+2H20?Fe(OH)2+2HCl;4Fe(OH)2+O2+2H2O=4Fe(OH)3;2Fe(OH)3
Fe2O3+3H2O,以此解答该题.
| ||
解答:
解:(1)除去盐酸获得亚铁盐,所加的金属只能是金属铁,故答案为:Fe;
(2)氯化亚铁溶液中亚铁离子会发生水解反应生成氢氧化亚铁,即FeCl2+2H2O?Fe(OH)2+2HCl,氢氧化亚铁不稳定,会被氧化为氢氧化铁,4Fe(OH)2+O2+2H2O=4 Fe(OH)3,氢氧化铁可以分解,即2Fe(OH)3
Fe2O3+3H2O,总方程式为4FeCl2+4H2O+O2
2Fe2O3+4HCl,
故答案为:4FeCl2+4H2O+O2
2Fe2O3+4HCl(或 FeCl2+2H20?Fe(OH)2+2HCl,4Fe(OH)2+O2+2H2O=4Fe(OH)3,2Fe(OH)3
Fe2O3+3H2O);
(3)氧化铜可以溶解于强酸溶液中,得到含有铜离子的盐,加入足量铁粉可以将金属铜置换出来,据此可以检验固体是氧化铜,氧化亚铁可以和强酸反应生成亚铁盐,能使高锰酸钾褪色,据此可以检验固体中含有氧化亚铁,
可取少量样品于试管中,加入足量的3mol?L-1H2SO4,充分振荡.
取少许上述溶液于,加入足量铁粉,充分振荡;再加入足量3mol?L-1H2SO4,充分振荡,
取少许步骤1溶液于试管中,逐滴加入0.01 mol?L-1酸性KMnO4溶液,
若试管中出现红色固体,说明试样中有CuO,如果紫红色褪去,说明试样中有FeO,
故答案为:
(4)设HCl体积为VL,则
=36.5%,解得V=224,
故答案为:224.
(2)氯化亚铁溶液中亚铁离子会发生水解反应生成氢氧化亚铁,即FeCl2+2H2O?Fe(OH)2+2HCl,氢氧化亚铁不稳定,会被氧化为氢氧化铁,4Fe(OH)2+O2+2H2O=4 Fe(OH)3,氢氧化铁可以分解,即2Fe(OH)3
| ||
| ||
故答案为:4FeCl2+4H2O+O2
| ||
| ||
(3)氧化铜可以溶解于强酸溶液中,得到含有铜离子的盐,加入足量铁粉可以将金属铜置换出来,据此可以检验固体是氧化铜,氧化亚铁可以和强酸反应生成亚铁盐,能使高锰酸钾褪色,据此可以检验固体中含有氧化亚铁,
可取少量样品于试管中,加入足量的3mol?L-1H2SO4,充分振荡.
取少许上述溶液于,加入足量铁粉,充分振荡;再加入足量3mol?L-1H2SO4,充分振荡,
取少许步骤1溶液于试管中,逐滴加入0.01 mol?L-1酸性KMnO4溶液,
若试管中出现红色固体,说明试样中有CuO,如果紫红色褪去,说明试样中有FeO,
故答案为:
| 操作步骤 | 预期现象和结论 |
| 步骤1.取少量样品于试管1中,加入足量的3mol?L-1H2SO4,充分振荡. | |
| 步骤2.取少许上述溶液于试管2,加入足量铁粉,充分振荡;再加入足量3mol?L-1H2SO4,充分振荡. 步骤3.取少许步骤1溶液于试管中3,逐滴加入0.01 mol?L-1酸性KMnO4溶液. (步骤2和步骤3的操作和现象结论可以互换位置) | 若试管中出现红色固体,说明试样中有CuO 如果紫红色褪去,说明试样中有FeO |
| ||
|
故答案为:224.
点评:本题考查了实验探究物质分离方法和物质性质的分析判断,为高频考点,侧重于学生的分析能力、实验能力和计算能力的考查,注意把握实验原理、掌握物质性质是关键,题目难度中等.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、(NH4)2SO4和CuSO4溶液都能使蛋白质沉淀析出 |
B、苯酚与甲醛在酸性条件下生成酚醛树脂的结构简式为 |
| C、醋酸和硬脂酸互为同系物,C6H14和C9H20也一定互为同系物 |
D、叶酸的结构为 ,它可以发生酯化、水解、加成等反应 ,它可以发生酯化、水解、加成等反应 |
铁有δ、γ、α三种晶体结构,以下依次是δ、γ、α三种晶体不同温度下转化的图示,下列有关说法不正确的是( )
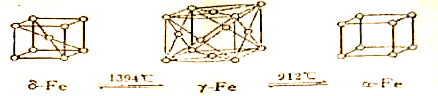

| A、δ-Fe晶体中与相邻铁原子距离相等且最近的铁原子有8个 |
| B、γ-Fe晶体中与相邻铁原子距离相等且最近的铁原子有12个 |
| C、将铁加热到1500℃分别急速冷却和缓慢冷却,得到的晶体结构不相同,但化学性质几乎相同 |
| D、α-Fe晶胞边长若为a cm,γ-Fe晶胞边长若为b cm,则α-Fe和γ-Fe两种晶体的密度比为b3:a3 |
 (1)判断含氧酸酸性强弱的一条经验规律是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性就越强.含氧酸酸性强弱与非羟基氧原子数的关系如下表所示:
(1)判断含氧酸酸性强弱的一条经验规律是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性就越强.含氧酸酸性强弱与非羟基氧原子数的关系如下表所示: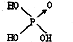
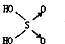
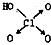

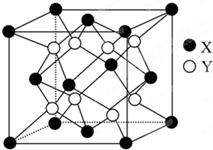 某离子晶体的晶体结构如图所示,试求:
某离子晶体的晶体结构如图所示,试求: