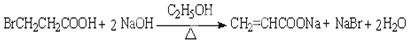题目内容
8.有A、B、C、D四种短周期元素,原子序数依次增大,已知A和C原子最外层只有一个电子,C燃烧时焰色反应是黄色,C单质在B单质中充分燃烧后生成一种淡黄色的固态化合物,A单质可以和D单质发生化合反应,且反应条件可以是点燃或者光照,根据以上叙述回答:(1)写出A、B、C的元素名称:A氢 B氧 C钠
(2)写出化学方程式:
①C+B2Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$Na2O2
②A+DH2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl.
分析 已知A和C原子最外层只有一个电子,说明A和C为第ⅠA族元素,C燃烧时的焰色反应是黄色,则C为Na元素,C的单质在高温下与B的单质充分反应可以产生淡黄色固态化合物,可知B为O元素,生成的淡黄色固体为过氧化钠,A单质与D单质可以发生化合反应,且反应条件可以是点燃或者光照,应为氢气与氯气的反应,则A为H元素,D为Cl元素,以此解答该题.
解答 解:已知A和C原子最外层只有一个电子,说明A和C为第ⅠA族元素,C燃烧时的焰色反应是黄色,则C为Na元素,C的单质在高温下与B的单质充分反应可以产生淡黄色固态化合物,可知B为O元素,生成的淡黄色固体为过氧化钠,A单质与D单质可以发生化合反应,且反应条件可以是点燃或者光照,应为氢气与氯气的反应,则A为H元素,D为Cl元素,
(1)由以上分析可知A、B、C的元素名称分别为氢、氧、钠,故答案为:氢;氧;钠;
(2)钠在加热条件下和氧气反应生成过氧化钠,反应方程式为2Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$Na2O2,
氢气与氯气反应生成氯化氢,反应的方程式为H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl,
故答案为:2Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$Na2O2;H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl.
点评 本题以元素的推断为载体考查了元素化合物的性质,为高考常见题型,侧重于学生的分析能力的考查,难度不大,能正确推断元素是解本题的关键,注意把握物质的结构和性质,为解答该题的关键.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
19.已知NA为阿伏伽德罗常数,下列叙述正确的是( )
| A. | 标准状况下,2.24L H2O含有的分子数为0.1NA | |
| B. | 标准状况下,2.24L H2 含有的分子数为0.1mol | |
| C. | 分子数为NA 的CO和N2混合气体的体积约为22.4L,质量为28g | |
| D. | 1mol CH4分子中所含的电子总数为10 NA |
16.下列变化属于化学变化的是( )
| A. | 煤的干馏 | B. | 石油的分馏 | C. | 海水的蒸馏 | D. | 萃取 |
3.下列叙述正确的是( )
| A. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 由于石墨转化为金刚石是吸热反应,所以金刚石比石墨稳定 | |
| C. | 在稀溶液中,强酸与强碱反应生成1molH2O将吸收57.3kJ热量 | |
| D. | 在101kPa时,2g氢气完全燃烧生成液态水放出285.8kJ热量,则等质量的氢气完全燃烧生成气态水时放出热量将小于285.8kJ |
13.下列实验装置或操作能达到实验目的是( )
| A. | 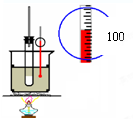 实验室制硝基苯 | B. | 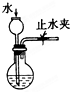 检查装置气密性 | ||
| C. | 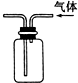 利用排空气法收集丙烷 | D. | 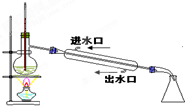 石油分馏 |
17.今有吸热反应C+CO2?2CO和放热反应N2+3H2?2NH3,两者的反应速率为分别为V1和V2,当温度升高时,V1和V2的变化情况为( )
| A. | 同时增大 | B. | 同时减少 | C. | V1增大,V2减小 | D. | V1减小,V2增大 |
18.化学与我们的生活息息相关,下列有关基本营养物质的说法正确的是( )
| A. | 人体内没有水解纤维素的酶,所以纤维素在人体内没有任何作用 | |
| B. | 变质的油脂有难闻的哈喇味是因为油脂发生了加成反应 | |
| C. | 吃馒头时越嚼越感觉甜是因为淀粉发生了水解反应 | |
| D. | 牛奶中含有丰富的蛋白质,所以羊毛衫上沾有奶渍时可以用加酶洗衣粉洗涤 |
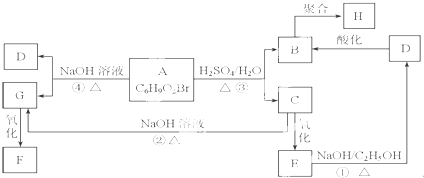
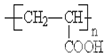 ;
;