题目内容
1.在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中大量共存的是( )| A. | 滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl-、CH3COO- | |
| B. | pH值为1的溶液:Cu2+、Na+、Mg2+、NO3- | |
| C. | 水电离出来的c(H+)=10-12mol/L的溶液:K+、HCO3-、Br-、Ba2+ | |
| D. | 所含溶质为Na2CO3的溶液:K+、Ca2+、NO3-、Al3+ |
分析 A.滴加石蕊试液显红色的溶液中存在大量氢离子,醋酸根离子与氢离子反应;
B.该溶液为酸性溶液,四种离子之间不反应,都不与氢离子反应;
C.水电离出来的c(H+)=10-12mol/L的溶液中存在大量氢离子或氢氧根离子,碳酸氢根离子与氢离子、氢氧根离子;
D.碳酸钠与钙离子、铝离子发生反应.
解答 解:A.滴加石蕊试液显红色的溶液中存在大量氢氧根离子,CH3COO-与氢离子反应,在溶液中不能大量共存,故A错误;
B.pH值为1的溶液中存在大量氢离子,Cu2+、Na+、Mg2+、NO3-之间不发生反应,都不与氢离子反应,在溶液中能够大量共存,故B正确;
C.水电离出来的c(H+)=10-12mol/L的溶液中存在大量氢离子或氢氧根离子,HCO3-与氢离子和氢氧根离子反应,在溶液中不能大量共存,故C错误;
D.Na2CO3的溶液与Ca2+、Al3+之间发生反应,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,为高考的高频题,题目难度中等,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间;能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在;溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”等.

练习册系列答案
相关题目
11.常温下,将pH=2的酸溶液和pH=12的苛性钠溶液等体积混合后,则溶液中( )
| A. | pH=7 | B. | pH≥7 | C. | pH≤7 | D. | C(H+)•C(OH-)=10-14 |
12.某合作学习小组讨论辨析以下说法:
①粗盐和酸雨都是混合物;
②金属氧化物都是碱性氧化物;
③冰和干冰既是纯净物又是化合物;
④不锈钢和目前流通的硬币都是合金;
⑤盐酸和食醋既是化合物又是酸;
⑥纯碱和熟石灰都是碱;
⑦豆浆和雾都是胶体.
上述说法正确的是( )
①粗盐和酸雨都是混合物;
②金属氧化物都是碱性氧化物;
③冰和干冰既是纯净物又是化合物;
④不锈钢和目前流通的硬币都是合金;
⑤盐酸和食醋既是化合物又是酸;
⑥纯碱和熟石灰都是碱;
⑦豆浆和雾都是胶体.
上述说法正确的是( )
| A. | ①②③④ | B. | ①②⑤⑥ | C. | ③⑤⑥⑦ | D. | ①③④⑦ |
9.下列关于硅元素及其化合物的有关说法正确的是( )
| A. | 硅可用于制光导纤维 | |
| B. | SiO2+3C$\frac{\underline{\;高温\;}}{\;}$SiC+2CO↑中碳只做还原剂 | |
| C. | 因为玻璃中含有SiO2,所以不能用磨口玻璃塞的试剂瓶盛装碱性溶液 | |
| D. | SiO2能与氢氧化钠溶液和氢氟酸反应,所以SiO2是两性氧化物 |
16.下列物质中属于电解质,但在给定条件下不能导电的是( )
| A. | 液态溴化氢 | B. | 液氨 | C. | 铝 | D. | 稀硝酸 |
6.下列说法正确的是( )
| A. | 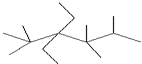 的系统命名为2,2,4,4,5-五甲基-3-二乙基己烷 的系统命名为2,2,4,4,5-五甲基-3-二乙基己烷 | |
| B. | 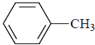 能使KMnO4溶液褪色,说明苯环与甲基相连的碳碳单键变得活泼,被KMnO4氧化而断裂 能使KMnO4溶液褪色,说明苯环与甲基相连的碳碳单键变得活泼,被KMnO4氧化而断裂 | |
| C. | 等物质的量的乙烯和乙醇的耗氧量相同 | |
| D. | 石油的分馏和煤的干馏都是物理变化 |
10.分子式为C10H20O2的有机物A,能在故性条件下水解生成有机物C和D.且C 在一定条件下可转化成D,则A的可能结构有( )
| A. | 4种 | B. | 6 种 | C. | 3 种 | D. | 5 种 |
11. 常温下,向20ml 0.1mol/L 酒石酸(用H2T表示)溶液中逐渐滴加等物质的量浓度的NaOH溶液.有关微粒的物质的量与混合溶液的pH有如图关系,下列说法正确的是( )
常温下,向20ml 0.1mol/L 酒石酸(用H2T表示)溶液中逐渐滴加等物质的量浓度的NaOH溶液.有关微粒的物质的量与混合溶液的pH有如图关系,下列说法正确的是( )
 常温下,向20ml 0.1mol/L 酒石酸(用H2T表示)溶液中逐渐滴加等物质的量浓度的NaOH溶液.有关微粒的物质的量与混合溶液的pH有如图关系,下列说法正确的是( )
常温下,向20ml 0.1mol/L 酒石酸(用H2T表示)溶液中逐渐滴加等物质的量浓度的NaOH溶液.有关微粒的物质的量与混合溶液的pH有如图关系,下列说法正确的是( )| A. | HT-在溶液中水解程度大于电离程度 | |
| B. | 当V(NaOH)=20mL时,溶液中水的电离程度比纯水大 | |
| C. | 当V(NaOH)=30mL时,溶液中存在c(Na+)>c(HT-)>c(T2-)>c(OH-)>c(H+) | |
| D. | 当V(NaOH)=40ml时,溶液中存在c(OH-)=c(HT-)+2 c(H2T)+c(H+) |