题目内容
6.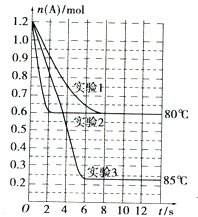 将1.2mol的A气体充入2L恒容密闭容器中发生反应:A(g)?2B(g).在三种不同条件下进行实验,A的物质的量随时间的变化如图所示.试回答下列问题:
将1.2mol的A气体充入2L恒容密闭容器中发生反应:A(g)?2B(g).在三种不同条件下进行实验,A的物质的量随时间的变化如图所示.试回答下列问题:(1)实验1中,4s时A的转化率为37.5%;此条件下该反应的平衡常数K1的值为1.2mol/L.
(2)实验2与实验1对比,其可能隐含的反应条件是使用催化剂.
(3)根据实验3与实验1的图象比较,可推测该反应是吸热(填“放热”或“吸热”)反应.设实验1~3的平衡常数的值分别为K1、K2、K3,则它们之间的关系为K1=K2<K3(填“>”、“<”或“=”).
(4)为了验证增大催化剂的表面积、增大压强可提高化学反应速率这一结论,某同学在实验1的基础上又利用该容器设计了实验4和实验5,部分实验条件及数据见下表.请将表格补充完整
| 实验编号 及其目的 | V(容积)/L | t/℃ | n(A起始)/mol | n(B起始)/mol | 催化剂的质量/g | 催化剂的表面积/m2•g-1[来源:Z.xx.k.Com] |
| 实验1 参照对比实验 | 2 | 80 | 1.2 | 0 | a | b |
| 实验4:催化剂的表面积对反应速率的影响 | | | | | | |
| 实验5目的: | 1 | | | | | |
分析 (1)A的转化率=$\frac{A的浓度变化量}{A的起始浓度}$×100%;依据化学方程式计算平衡浓度,结合平衡常数概念是利用生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积得到;
(2)实验2与实验1对比,反应都从浓度为0.6mol/LA的反应开始建立平衡,温度相同,平衡时B的浓度相同,到达平衡的时间实验2比实验1少,只能是实验2使用催化剂;
(3)根据温度对化学平衡的影响判断;结合图表中平衡常数随温度变化分析K1、K2、K3它们之间的关系;
(4)根据该实验室为了验证增大催化剂的表面积、压强可提高化学反应速率这一结论分析,实验5目的:探究压强对反应速率的影响.
解答 解:(1)根据图象可知:A的转化率=$\frac{A的浓度变化量}{A的起始浓度}$×100%=$\frac{0.225mol•{L}^{-1}}{0.6mol{•L}^{-1}}$×100%=37.5%;
80℃时 A(g)?2B(g).
起始量(mol) 1.2 0
变化量(mol) 0.6 1.2
平衡量(mol) 0.6 1.2
反应平衡常数K=$\frac{{c}^{2}(B)}{c(A)}$=$\frac{(\frac{1.2mol}{2L})^{2}}{\frac{0.6mol}{2L}}$═1.2mol/L,
故答案为:37.5%;1.2mol/L;
(2)实验2和实验1相比,反应都从浓度为0.6mol/LA的反应开始建立平衡,温度相同,平衡时B的浓度相同,到达平衡的时间实验2比实验1少,即条件改变只加快反应速率,不影响平衡移动,反应前后为气体体积增加的反应,故只能是实验2使用催化剂,
故答案为:使用催化剂;
(3)根据实验3与实验1的图象比较,可看出升高温度,A的平衡浓度减小,说明升高温度平衡向正反应方向移动,故正反应是吸热反应,平衡常数只随温度变化,实验2与实验1温度相同,所以K1=K2,
正反应是吸热反应,升高温度向正反应方向进行,实验3反应温度为85℃,大于实验1与实验2温度,所以生成物浓度大,平衡常数大,所以K2<K3,
故答案为:吸热;=;<;
(4)实验4:目的是探究催化剂的表面积对反应速率的影响,所以只改变催化剂比表面积,探究催化剂比表面积对化学反应速率的影响,其它参数不变,可将催化剂的表面积变为2b(或nb(n>1)),该实验室为了验证增大催化剂的表面积、压强可提高化学反应速率这一结论分析,实验5目的:探究压强对反应速率的影响,所以通过改变容器的体积来实现,所以各数据如下,
故答案为:
| 实验编号及其目的 | V(容积)/L | t/℃ | n(A起始)/mol | n(B起始)/mol | 催化剂的质量/g | 催化剂的表面积/m2•g-1 |
| 2 | 80 | 1.2 | 0 | a | 2b(或nb(n>1)) | |
| 实验5目的: 压强对反应速率的影响 | 80 | 1.2 | 0 | a | b |
点评 本题以图象为载体考查平衡影响因素、平衡常数的计算、读图提取信息能力,题目难度中等,注意结合图的信息运用知识解决问题.

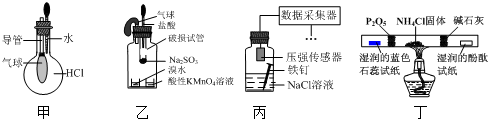
| A. | 用装置甲验证HCl气体易溶于水 | |
| B. | 用装置乙验证SO2具有漂白性 | |
| C. | 用装置丙采集到的压强数据判断铁钉发生析氢腐蚀还是吸氧腐蚀 | |
| D. | 用装置丁检验NH4Cl分解产生的气体 |
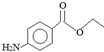
| A. | M分子式为C8H11NO2 | |
| B. | 1mol M与NaOH溶液反应消耗1mol NaOH | |
| C. | M与盐酸的反应属于加成反应 | |
| D. | 与M含有相同官能团的同分异构体有8种 |
 甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素(化学方程式为:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O).
甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素(化学方程式为:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O).(1)请写出该反应对应的离子方程式(提示:H2C2O4是弱酸):2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.
设计实验方案如下(实验中所用KMnO4溶液均已加入H2SO4):
(2)甲组:通过测定单位时间内生成CO2气体体积的大小来比较化学反应速率的大小.
实验装置如图,实验时分液漏斗中A溶液一次性放下,A、B的成分见表:
| 序号 | T (K) | 催化剂用量(g) | A溶液 | B溶液 |
| ①① | 298 | 0 | 2mL 0.2mol/L H2C2O4溶液 | 4mL 0.001mol/L KMnO4溶液 |
| ②② | 298 | 0 | 2mL 0.2mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4溶液 |
| ③③ | 323 | 0.5 | 2mL 0.2mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4溶液 |
| ④④ | 298 | 0.5 | 2mL 0.2mol/L H2C2O4溶液 | 4mL 0.01mol/L KMnO4溶液 |
(3)乙组:通过测定KMnO4溶液褪色所需时间的多少来比较化学反应速率的大小.取两支试管对实验①和②分别进行三次实验,测得以下实验数据(从混合振荡均匀开始计时):
| 实验序号 | 溶液褪色所需时间t(min) | ||
| 第一次 | 第二次 | 第三次 | |
| ①① | 6 | 7 | 7 |
| ②② | 14 | 11 | 14 |
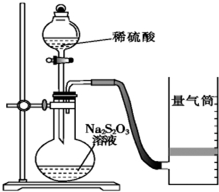 化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.
化学反应速率是描述化学反应进行快慢程度的物理量.下面是某同学测定化学反应速率并探究其影响因素的实验.Ⅰ.测定化学反应速率
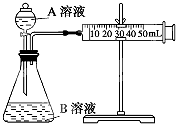
该同学利用如图装置测定化学反应速率.
(已知:S2O32-+2H+═H2O+S↓+SO2↑)
(1)为保证实验准确性、可靠性,利用该装置进行实验前应先进行的步骤是检查装置的气密性;除如图装置所示的实验用品、仪器外,还需要的一件实验仪器是秒表.
(2)若在2min时收集到224mL(已折算成标准状况)气体,可计算出该2min内H+的反应速率,而该测定值比实际值偏小,其原因是SO2会部分溶于水,导致所测得SO2体积偏小.
(3)试简述测定该反应的化学反应速率的其他方法:测定一段时间内生成硫单质的质量或测定一定时间内溶液H+浓度的变化 (写一种).
Ⅱ.为探讨反应物浓度对化学反应速率的影响,设计的实验方案如表.
(已知 I2+2S2O32-═S4O62-+2I-,其中Na2S2O3溶液均足量)
| 实验序号 | 体积V/mL | 时间/s | |||
| Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
| ① | 10.0 | 2.0 | 4.0 | 0.0 | t1 |
| ② | 8.0 | 2.0 | 4.0 | 2.0 | t2 |
| ③ | 6.0 | 2.0 | 4.0 | Vx | |
| A. | 水属于氧化物 | B. | 水分子中含有非极性键 | ||
| C. | 冰与可燃冰的化学成分完全相同 | D. | 氟气与水的反应中,水作氧化剂 |
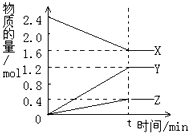 在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.依图所示:
在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.依图所示: