题目内容
5.下列元素相关粒子的电子排布式中,前者一定是金属元素,后者一定是非金属元素的是( )| A. | 3s1 3s2 | B. | 4s1 3s23p4 | C. | 3s2 4s2 | D. | 2s22p4 3s23p5 |
分析 题中能级数为3的位于第三周期,根据电子排布式可确定元素种类,能级为4的元素,可能为主族、也可能为副族,以此解答该题.
解答 解:A.3s1为Na元素,3s2为Mg元素,都为金属,故A错误;
B.4s1可能为K或过渡金属元素,3s23p4为S元素,故B正确;
C.3s2为Mg,4s2可能为Ca或过渡金属元素,都为金属元素,故C错误;
D.2s22p4为S元素,3s23p5为Cl元素,都为非金属元素,故D错误.
故选B.
点评 本题考查核外电子排布、原子结构与元素性质等,为高频考点,侧重考查学生的分析能力,比较基础,关键根据核外电子排布确定元素,有利于基础知识的巩固.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.下列有机物,按沸点由高到低的顺序排列正确的是( )
①庚烷 ②己烷 ③正戊烷 ④新戊烷 ⑤异丁烷.
①庚烷 ②己烷 ③正戊烷 ④新戊烷 ⑤异丁烷.
| A. | ①>②>③>④>⑤ | B. | ⑤>④>③>②>① | C. | ①>②>④>③>⑤ | D. | ①>②>③>⑤>④ |
16.关于Na2O2+SO2=Na2SO4的说法正确的是( )
| A. | Na2O2做氧化剂 | B. | Na2O2做还原剂 | ||
| C. | Na2O2既做氧化剂又做还原剂 | D. | Na2O2既不做氧化剂又不做还原剂 |
13.没有做实验而欺骗老师的学生是( )
| A. | 老师,我用Na2SO3与BaCl2溶液作用,有白色沉淀生成,加入盐酸后沉淀消失 | |
| B. | 我向BaCl2溶液中通入SO2气体,也有白色沉淀生成 | |
| C. | 老师,我向Ba(OH)2溶液中通入SO2气体,也有白色沉淀生成老师 | |
| D. | 老师,我向用硝酸酸化的BaCl2溶液中通入SO2气体,我以为不会有沉淀,可出现了白色沉淀 |
20.共价键、离子键和范德华力是构成物质微粒间的不同作用力,下列物质中只含有上述一种作用力的是( )
| A. | 干冰 | B. | 氯化钠 | C. | 氢氧化钠 | D. | 冰 |
17.CuCl常用作有机合成催化剂,实验室以初级铜矿粉(主要含Cu2S及少量Fe2O3、FeO等)为原料制备活性CuCl.实验过程如图:
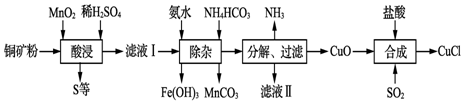
(1)“酸浸”中,加入稀H2SO4不宜过量太多的原因是避免“除杂”步骤消耗更多的氨水和NH4HCO3.
(2)已知:Cu(OH)2可溶于氨水形成深蓝色[Cu(NH3)4]2+溶液.
①“分解”实验条件及现象如表所示.
则“分解”实验条件应选C(填序号).
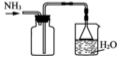
②“分解”生成的NH3可以回收利用.在实验室用图装置来收集NH3,当集气瓶收集满NH3时观察到的现象是漏斗中的液面忽上忽下.
(3)CuCl易氧化,Ksp(CuCl)=1.2×10-6.“合成”中生成CuCl的离子方程式为SO2+2CuO+2Cl-═2CuCl+SO42-;请补充从“合成”所得混合物中得到CuCl的实验操作步骤:过滤、洗涤、真空干燥或隔绝空气干燥
(4)请补充“除杂”步骤中分别回收Fe(OH)3和MnCO3的实验方案:向“滤液Ⅰ”中边搅拌边滴加氨水至溶液pH为[3.2,4.7),将所得沉淀过滤、洗涤、干燥得Fe(OH)3.再向滤液中边搅拌边滴加氨水和碳酸氢铵混合溶液至pH=10,有大量MnCO3沉淀生成,将沉淀过滤、洗涤、干燥得MnCO3.
【已知:pH=3.2时,Fe(OH)3沉淀完全;pH=4.7时,Cu(OH)2开始沉淀;pH=10时,MnCO3沉淀完全】

(1)“酸浸”中,加入稀H2SO4不宜过量太多的原因是避免“除杂”步骤消耗更多的氨水和NH4HCO3.
(2)已知:Cu(OH)2可溶于氨水形成深蓝色[Cu(NH3)4]2+溶液.
①“分解”实验条件及现象如表所示.
| 序号 | 温度/℃ | 压强/kPa | 时间/min | 残液颜色 |
| A | 110 | 101.3 | 60 | 浅蓝色 |
| B | 100 | 74.6 | 40 | 很浅 |
| C | 90 | 60.0 | 30 | 无色透明 |
②“分解”生成的NH3可以回收利用.在实验室用图装置来收集NH3,当集气瓶收集满NH3时观察到的现象是漏斗中的液面忽上忽下.

(3)CuCl易氧化,Ksp(CuCl)=1.2×10-6.“合成”中生成CuCl的离子方程式为SO2+2CuO+2Cl-═2CuCl+SO42-;请补充从“合成”所得混合物中得到CuCl的实验操作步骤:过滤、洗涤、真空干燥或隔绝空气干燥
(4)请补充“除杂”步骤中分别回收Fe(OH)3和MnCO3的实验方案:向“滤液Ⅰ”中边搅拌边滴加氨水至溶液pH为[3.2,4.7),将所得沉淀过滤、洗涤、干燥得Fe(OH)3.再向滤液中边搅拌边滴加氨水和碳酸氢铵混合溶液至pH=10,有大量MnCO3沉淀生成,将沉淀过滤、洗涤、干燥得MnCO3.
【已知:pH=3.2时,Fe(OH)3沉淀完全;pH=4.7时,Cu(OH)2开始沉淀;pH=10时,MnCO3沉淀完全】
14.将3mol X和2.5mol Y混合于2L密闭容器中,发生如下反应:3X(g)+Y(g)?nZ(g)+2W(g),5min达到平衡状态,生成1mol W,经测定以Z表示的平均反应速率为0.1mol/(L•min),则下列结论错误的是( )
| A. | X表示的平均反应速率为0.3mol/(L•min) | |
| B. | n的值等于2 | |
| C. | 平衡时,Y的浓度为1mol/L | |
| D. | 平衡时,Y的转化率为20% |
10.下面对氯气的叙述,正确的是( )
| A. | 液氯可使湿的红布条褪色,所以液氯具有漂白性 | |
| B. | 氯气没有漂白性,但会使湿润的红色布条褪色 | |
| C. | 在通常情况下,氯气可以和任何金属直接化合 | |
| D. | 氯气有毒,可以用澄清的石灰水尾气吸收;久置的氯水最终变为稀盐酸 |