题目内容
4.下列各指定微粒的数目比是1:1的是( )| A. | Na2O2溶液中阴离子和阳离子 | |
| B. | NaHSO4溶液中阳离子和阴离子 | |
| C. | ${\;}_{12}^{24}$Mg2+离子中的质子和中子 | |
| D. | 氯化钠溶液中阳离子和阴离子的电子数 |
分析 A.Na2O2晶体中阴离子和阳离子分别为O22-和Na+;
B.NaHSO4晶体中阳离子和阴离子分别为Na+和HSO4-;
C.${\;}_{12}^{24}$Mg2+离子离子中的质子和中子分别为12;
D.氯化钠中阳离子Na+、阴离子Cl-两者电子总数不等.
解答 解:A.Na2O2晶体中阴离子和阳离子分别为O22-和Na+,二者比值为1:2,故A不选;
B.NaHSO4溶液中阳离子为Na+、H+,阴离子为SO42-,阳离子和阴离子比值为2:1,故B不选;
C.${\;}_{12}^{24}$Mg2+离子中的质子和中子分别为12,比值为1:1,故C选;
D.氯化钠中的阳离子Na+的电子数为10,阴离子Cl-电子数为17+1=18,比值为5:9,故D不选.
故选C.
点评 本题考查不同晶体的结构以及原子的构成等知识,为高考常见题型和高频考点,侧重于学生的分析能力和基本概念的综合理解和运用的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
12.工业上获得大量的乙烯、丙烯和甲烷,采用的方法是( )
| A. | 石油分馏 | B. | 石油裂化 | C. | 石油裂解 | D. | 通过沼气池制取 |
19.化学能与热能、电能等可以相互转化,关于化学能与其他能量相互转化的说法正确的是( )
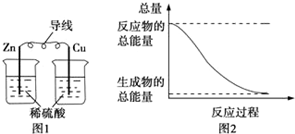

| A. | 图1所示的装置能将化学能转变为电能 | |
| B. | 图2所示的反应为吸热反应 | |
| C. | 化学反应中能量变化的主要原因是化学键的断裂与生成 | |
| D. | 中和反应中,反应物的总能量比生成物的总能量低 |
9.关于如图所示的原电池,下列说法正确的是( )
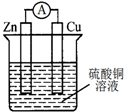

| A. | 电子从锌电极通过电流表流向铜电极 | |
| B. | 锌电极发生还原反应,铜电极发生氧化反应 | |
| C. | 反应后,锌电极的质量减小 | |
| D. | 铜电极作正极,发生的电极反应为2H++2e-═H2↑ |
16.下列叙述正确的是( )
| A. | 同主族元素自上而下金属性减弱 | |
| B. | 同主族元素自上而下,得电子能力增强 | |
| C. | 同周期元素中ⅠA族元素的原子半径最小 | |
| D. | 同周期元素中ⅦA元素气态氢化物最稳定 |
13.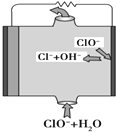 镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低等特点.一般研究的镁燃料电池可分为镁空气燃料电池、镁海水燃料电池、镁过氧化氢燃料电池和镁次氯酸盐燃料电池.其中,镁次氯酸盐燃料电池的工作原理如图所示,下列有关说法不正确的是( )
镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低等特点.一般研究的镁燃料电池可分为镁空气燃料电池、镁海水燃料电池、镁过氧化氢燃料电池和镁次氯酸盐燃料电池.其中,镁次氯酸盐燃料电池的工作原理如图所示,下列有关说法不正确的是( )
 镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低等特点.一般研究的镁燃料电池可分为镁空气燃料电池、镁海水燃料电池、镁过氧化氢燃料电池和镁次氯酸盐燃料电池.其中,镁次氯酸盐燃料电池的工作原理如图所示,下列有关说法不正确的是( )
镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低等特点.一般研究的镁燃料电池可分为镁空气燃料电池、镁海水燃料电池、镁过氧化氢燃料电池和镁次氯酸盐燃料电池.其中,镁次氯酸盐燃料电池的工作原理如图所示,下列有关说法不正确的是( )| A. | 镁燃料电池中镁均为负极,发生氧化反应 | |
| B. | 镁次氯酸盐燃料电池的总反应式为Mg+ClO-+H2O═Mg(OH)2+Cl- | |
| C. | 镁过氧化氢燃料电池,酸性电解质中正极反应式为H2O2+2H++2e-═2H2O | |
| D. | 镁次氯酸盐燃料放电过程中OH-移向正极 |
14.已知:物质的能量越低越稳定,白磷转化为红磷是放热的,据此下列说法中正确的是( )
| A. | 白磷转化为红磷是物理变化 | |
| B. | 在相同条件下红磷比白磷稳定 | |
| C. | 相同条件下,红磷所具有的总能量比白磷的高 | |
| D. | 相同质量的红磷和白磷完全燃烧放出的能量相等 |