��Ŀ����
��ҵ�Ͻ�����ұ�����̸��ӡ�
��1�������漰��2���Ȼ�ѧ����ʽ��
 ��H=��15.73kJ��mol��1
��H=��15.73kJ��mol��1
Fe3O4(s)��CO(g) = 3FeO(s)��CO2(g) ��H= +640.4kJ��mol��1
��ӦFe2O3(s)��CO(g) = 2FeO(s)��CO2(g) ����H= ��
��2����ҵ�ϵ������п��Һ��ʵ��ʪ����п������������ʹH���ѷŵ硢�����缫���ܽ�)��д������ܷ���ʽ ��
��3�����ɾ�����Ƭ�������ڵ�Һ̬пˮ�п��Ƶö�п�ְ壬���ְָ���к�ǿ����ʴ��������п�ְ�ĶƲ�һ�����ƻ���п����Ϊԭ��ص� ������ ��Ӧ�������������ԭ����
��4��ʵ�����ö�п�ְ���ϡ������ȡ��״���µ�����4.48L����÷�Ӧת�Ƶĵ�����Ϊ ��������������ʵ����� ��
��1����H= +411.20kJ��mol��1(2) 2ZnSO4��2H2O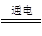 2Zn��O2����2H2SO4(3) ��������
2Zn��O2����2H2SO4(3) ��������
(4) 0.4NA 0.2mol
��������
�����������1���ɸ�˹���ɵ���H=��-15.73+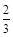 ��640.4��kJ��mol��1=+411.20kJ��mol��1����2���������п��Һ��п��������ӦΪ2H2O-4e-=4H++O2����������ӦΪZn2++2e-=Zn���ܷ�ӦΪ2ZnSO4��2H2O
��640.4��kJ��mol��1=+411.20kJ��mol��1����2���������п��Һ��п��������ӦΪ2H2O-4e-=4H++O2����������ӦΪZn2++2e-=Zn���ܷ�ӦΪ2ZnSO4��2H2O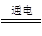 2Zn��O2����2H2SO4����3��п�������ã�п�����γ�ԭ���ʱ��п������������������4��Zn+H2SO4=ZnSO4+H2����Fe+H2SO4=FeSO4+H2����ÿ����1molH2��ת�Ƶ���2mol����������1mol��
2Zn��O2����2H2SO4����3��п�������ã�п�����γ�ԭ���ʱ��п������������������4��Zn+H2SO4=ZnSO4+H2����Fe+H2SO4=FeSO4+H2����ÿ����1molH2��ת�Ƶ���2mol����������1mol��
���㣺��˹���� �绯ѧ ��ѧ����
������ԭ����У�һ�������ǿ����������ʧ���ӣ�������������������Ӧ��

 ����ͬ�����Ծ�ϵ�д�
����ͬ�����Ծ�ϵ�д� ��H=��15.73kJ��mol��1
��H=��15.73kJ��mol��1

 ��
�� ��
�� �ѷŵ硢�����缫���ܽ�)��д������ܷ���ʽ
��
�ѷŵ硢�����缫���ܽ�)��д������ܷ���ʽ
��