题目内容
15. 现有常温时浓度相同的五种电解质溶液:①CH3COOH ②Na2CO3 ③HNO3④CH3COONa ⑤NaOH
现有常温时浓度相同的五种电解质溶液:①CH3COOH ②Na2CO3 ③HNO3④CH3COONa ⑤NaOH(1)五种溶质中是弱电解质的是①(填编号),若常温时该弱电解质电离常数为K,1mol/L的该溶液中c(H+)约为$\sqrt{K}$mol/L(用K表示)
(2)④溶液中离子与分子共6种(包括水分子).
(3)这五种溶液的pH由小到大的顺序是③<①<④<②<⑤(填编号).
(4)将 CH3COONa溶液稀释100倍时,其pH变化如图中B曲线(填字母).
分析 (1)弱酸、弱碱、水都属于弱电解质;根据K=$\frac{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}{c(C{H}_{3}COOH)}$计算;
(2)根据CH3COONa 溶液中的水解和电离方程分析;
(3)盐溶液中溶质浓度相同,酸越弱,其盐的酸根水解程度越大,碱性越强,强酸强碱完全电离,弱酸弱碱部分电离;
(4)将 CH3COONa溶液稀释100倍时,pH变化小于2个单位.
解答 解:(1)弱酸、弱碱、水都属于弱电解质,则①CH3COOH ②Na2CO3 ③HNO3④CH3COONa ⑤NaOH中属于弱电解质的是①CH3COOH;1mol/L的该溶液中c(H+)=c(CH3COO-),由K=$\frac{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}{c(C{H}_{3}COOH)}$可得c(H+)=$\sqrt{K}$mol/L;
故答案为:①;$\sqrt{K}$;
(2)CH3COONa 溶液中的水解方程为CH3COO-+H2O?CH3COOH+OH-,电离方程为H2O?H++OH-,则溶液中离子与分子有CH3COOH、H2O、Na+、CH3COO-、H+、OH-,共6种;
故答案为:6;
(3)氢氧化钠是强碱,不水解,相同浓度的溶液氢氧化钠的pH最大,已知酸性:CH3COOH>H2CO3,所以碳酸钠的水解程度大于醋酸钠,碱性顺序:碳酸钠>醋酸钠,醋酸和硝酸均为酸,pH小于7,硝酸为强酸,完全电离,醋酸部分电离,综上知道五种溶液的pH由小到大的顺序是③<①<④<②<⑤,
故答案为:③<①<④<②<⑤;
(4)CH3COONa溶液显碱性,将 CH3COONa溶液稀释100倍时,pH变化小于2个单位,所以B符合;
故答案为:B.
点评 本题考查盐类的水解、弱电解质的电离、电离平衡常数的应用等,注意盐溶液的碱性强弱取决于阴离子的水解能力,当pH相同时,越难水解的盐,其浓度越大,难度中等,侧重于考查学生对基础知识的应用能力.

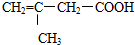 的结构,它不可能发生的反应是( )
的结构,它不可能发生的反应是( )| A. | 与银氨溶液反应析出银 | |
| B. | 使溴的四氯化碳溶液褪色 | |
| C. | 与乙醇在浓硫酸催化下发生酯化反应 | |
| D. | 与新制氢氧化铜反应 |
(1)N、Al、Si、Zn、Fe五种元素中,有一种元素的电离能数据如下:
| 电离能 | I1 | I2 | I3 | I4 | … |
| Im/kJ•mol-1 | 578 | 1817 | 2745 | 11578 | … |
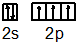 .
.(2)已知Zn2+能与氨分子形成配离子[Zn(NH3)4]2+,1mol该离子含有σ键的数目为15NA;
(3)K3[Fe(CN)6]可用来检验Fe2+,向硫酸亚铁溶液中加入几滴K3[Fe(CN)6],观察到的现象是产生蓝色沉淀,与CN-互为等电子体的微粒有CO、N2等(填化学式,写2种)
C、N、O三种元素第一电离能由大到小的顺序为N>O>C;三种元素形成的简单氢化物分子中键角由大到小依次为CH4>NH3>H2O(用分子式表示).
(4)已知Fe的相对原子质量为M,阿佛加德罗常数用NA表示,已知金属Fe为体心立方堆积,若Fe原子半径为acm,密度为ρg/cm3.则M=$\frac{32ρ{a}^{3}{N}_{A}}{3\sqrt{3}}$(用ρ、a、NA表达式表示)
| A. | 氯气溶于水:H2O+Cl2═2H++ClOˉ+Clˉ | |
| B. | 锌片插入稀H2SO4溶液中:Zn+2H+═Zn2++H2↑ | |
| C. | 氢氧化钡溶液与稀硫酸反应:H++SO42-+OH-+Ba2+═H2O+BaSO4↓ | |
| D. | 碳酸钙溶于稀盐酸:CO32-+2H+═H2O+CO2↑ |
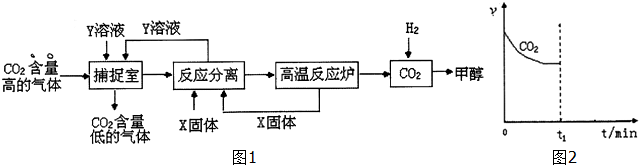
(1)下列有关捕捉空气中的CO2过程中的叙述不正确的有BD.
A、X选用CaO,而且要循环利用CaO与Y溶液
B、捕捉室里温度越高越有利于CO2 的捕捉
C、开放高效光催化剂分解水制氢气,是降低合成甲醇成本的有效途径
D、该捕捉CO2技术的应用有利于缓解全球变暖,而且能耗小
(2)在捕捉室用稀氨水喷淋“捕捉”空气中的CO2时,有NH2COONH4(氨基甲酸胺)生成.现将一定量纯净的氨基甲酸胺置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使反应
NH2COONH4(s)?2NH3(g)+CO2(g)达到分解平衡.实验测得不同温度及反应时间(t1<t2<t3)的有关表:氨基甲酸铵分解时温度、气体总浓度及反应时间的关系
 | 15 | 25 | 35 |
| 0 | 0 | 0 | 0 |
| t1 | 0.9×10-3 | 2.7×10-3 | 8.1×10-3 |
| t2 | 2.4×10-3 | 4.8×10-3 | 9.4×10-3 |
| t3 | 2.4×10-3 | 4.8×10-3 | 9.4×10-3 |
②根据表中数据换算出,15℃时合成反应2NH3(g)+CO2(g)?NH2COONH4(s)平衡常数K约为4.9×108.
(3)以捕捉到的CO2与H2为原料可合成甲醇(CH3OH),其反应的化学方程为:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g);△H<0.
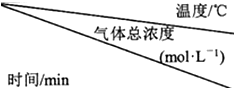
①将1mol CO2和3mol H2充入恒温恒压的密闭容器中发生上述反应,CO2消耗速率v(CO2)与时间关系如图2所示.若在时间t1时,向容器中再充入1mol CO2和3mol H2,请在图中画出CH3OH生成速率v(CH3OH)与时间的关系曲线.
②在一个恒温固定容积的密闭容器中,加入1mol CO2和3mol H2,充分反应后达到平衡放出热量为aKJ.若在原来的容器中加入2mol CO2和6mol H2,在相同温度下充分反应,达到平衡放出热量为bKJ.则a和b满足的关系b>2a.
| A. | 合金的熔点一般比组分金属高 | B. | 合金中只含金属元素 | ||
| C. | 合金的机械性能一般比组分金属好 | D. | 合金的硬度一般比组分小 |