题目内容
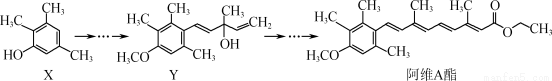
(10分)甲、乙、丙均为中学化学常见的气体单质,A、B、C为常见的化合物,A和B都极易溶于水,用玻璃棒分别蘸取A和B的浓溶液后,相互靠近会看到白烟。各物质之间存在如下图所示的转化关系:

请回答下列问题:
(1)丙与A反应生成乙和C的化学反应方程式为——————
(2)向0.1 mol/L的C溶液中通入A至显中性,溶液中各离子浓度由大到小的顺序为:__________.
(3)常温下取M的饱和溶液与AgI的饱和溶液等体积混合,再加入足量的AgNO3浓溶液发生反应,则生成沉淀的物质的量较多的是________。(填化学式)
(4)电解尿素[CO(NH2)2]的碱性溶液制取甲的装置示意图如右图(电解池中隔膜仅阻止气体通过,a、b极均为惰性电极)。

电解时,b极的电极反应是_______。若在a极产生112mL气体(标准状况),则消耗尿素的质量为______g。
(1)3Cl2+8NH3=6NH4Cl+N2;(2)c(NH4+)=c(Cl-)>c(OH-)=c(H+);(3)AgCl;
(4)CO(NH2)2+8OH--6e=CO32-+N2↑+6H2O;0.1
【解析】
试题分析:根据题意及物质之间的相互转化关系可知:甲是H2;乙是N2;丙是Cl2,A是NH3;B是HCl;C是NH4Cl;M是AgCl。(1)由于氧化性:Cl2>N2,所以丙与A反应生成乙和C的化学反应方程式为3Cl2+8NH3=6NH4Cl+N2;(2) NH4Cl是强酸弱碱盐,在溶液中NH4+发生水解反应消耗水电离产生的OH-,最终溶液显酸性。向0.1 mol/L的C溶液中通入A至显中性,根据电荷守恒可得:c(NH4+)+ c(H+)= c(Cl-)+c(OH-)。由于溶液显中性,所以c(H+)= c(OH-)。因此c(NH4+)=c(Cl-),盐电离程度远大于水的电离,因此溶液中各离子浓度由大到小的顺序为c(NH4+)=c(Cl-)>c(OH-)=c(H+);(3)常温下取M的饱和溶液与AgI的饱和溶液等体积混合,由于AgCl的溶解度大于AgI,所以溶液中c(Cl-)>c(I-),n(Cl-)>n(I-),所以再加入足量的AgNO3浓溶液发生反应,则生成沉淀的物质的量较多的是AgCl。(4)由于b电极进入KOH和尿素的混合溶液,从a电极区排除的反应溶液中无尿素,由于在尿素中N元素的化合价是-3价,所以发生氧化反应,b电极反应式是:CO(NH2)2+8OH--6e- =CO32-+N2↑+6H2O。在a电极区发生还原反应:2H++2e-=H2↑。n(H2)=0.112L÷22.4L/mol=0.005mol,转移电子的物质的量是0.005mol×2=0.01mol。在整个闭合回路中电子转移数目相等,m(CO(NH2)2)=[ 0.01mol÷6] ×60g/mol=0.1g。
考点:考查元素及化合物的推断、离子浓度大小比较、电解原理在气体制取中的应用的知识。

 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案(16分)草酸(H2C2O4)是一种二元弱酸,部分性质如下:能溶于水,易溶于乙醇;大约在175℃升华(175℃以上分解生成H2O、CO2和CO);H2C2O4+Ca(OH)2=CaC2O4↓+2H2O。现用H2C2O4进行如下实验:
(一) 探究草酸的不稳定性
通过如图实验装置验证草酸受热分解产物中的CO2和CO,A、B、C中所加入的试剂分别是:
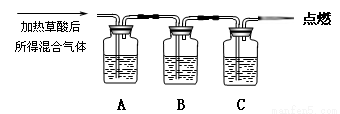
A、乙醇 B、 C、NaOH溶液。
(1)B中盛装的试剂 (填化学式)
(2)A中加入乙醇的目的是 。
(二) 探究草酸的酸性
将0.01mol草酸晶体(H2C2O4·2H2O)加入到100ml 0.2mol/L的NaOH溶液中充分反应,测得反应后溶液呈碱性,其原因是 (用离子方程式表示)。
(三) 用酸性KMnO4溶液与H2C2O4溶液反应来探究影响化学反应速率的因素
I、实验前先用酸性KMnO4标准溶液滴定未知浓度的草酸
反应原理: MnO4- + H2C2O4 + = Mn2+ + CO2↑+ H2O
(1)配平上述离子方程式。
(2)滴定时KMnO4溶液应盛装于 (填 “酸式”或“碱式”)滴定管中。
Ⅱ、探究影响化学反应速率的因素
实验组别 | c(H2C2O4) /(mol/L) | V(H2C2O4) /ml | c(KMnO4) /(mol/L) | V(KMnO4) /ml | c(H2SO4) /(mol/L) | 褪色所需时间 | 实验 目的 |
1 | 0.2 | 2 | 0.0025 | 4 | 0.12 | 6'55'' | (a) |
0.2 | 2 | 0.005 | 4 | 0.12 | 5'17'' | ||
0.2 | 2 | 0.01 | 4 | 0.12 | 3'20'' | ||
0.2 | 2 | 0.02 | 4 | 0.12 | 9'05'' | ||
0.2 | 2 | 0.03 | 4 | 0.12 | 11'33'' | ||
0.2 | 2 | 0.04 | 4 | 0.12 | 14'20'' |
下表列出了在“探究影响化学反应速率的因素”实验中得出的部分实验数据:
请回答:
(1)实验目的(a)是 ;
(2)根据表中数据在坐标中画出反应褪色所需时间随KMnO4溶液浓度的变化关系图像;
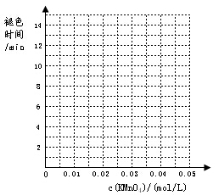
(3)若要探究催化剂对该反应速率的影响应选择MnSO4而不选MnCl2作为催化剂,其原因是 。