题目内容
3.下列描述中正确的是( )| A. | CS2为V形的极性分子 | |
| B. | ClO3-的空间构型为平面三角形 | |
| C. | CO32-VSEPR模型名称与离子的立体构型名称不一致 | |
| D. | SiF4和SO32-的中心原子均为sp3杂化 |
分析 A.根据价层电子对理论判断分子空间构型,结构不对称,正负电荷的中心不重合,为极性分子;
B.先求出中心原子的价层电子对数,再判断分子构型;
C.根据价电子对互斥理论,价层电子对个数=σ键个数+孤电子对个数.σ键个数=配原子个数分析;
D.先求出中心原子的价层电子对数,再判断杂化类型.
解答 解:A.CS2的结构为S=C=S,碳原子杂化轨道数为$\frac{1}{2}$×(4+0)=2,采取sp杂化,具有直线型结构的分子,结构对称,正负电荷的中心重合,为非极性分子,故A错误;
B.ClO3-中Cl的价层电子对数=3+$\frac{1}{2}$(7+1-2×3)=4,含有一个孤电子对,则离子的空间构型为三角锥形,故B错误;
C.CO32-的中心原子C原子上含有3个σ 键,中心原子上的孤电子对数=$\frac{1}{2}$(4+2-2×3)=0,所以CO32-的空间构型是平面三角形,VSEPR模型与分子立体结构模型一致,
故C错误;
D.SiF4中Si的价层电子对数=4+$\frac{1}{2}$(4-1×4)=4,SO32-中S的价层电子对数=3+$\frac{1}{2}$(6+2-2×3)=4,所以中心原子均为sp3杂化,故D正确.
故选C.
点评 本题考查分子的构型、原子杂化方式判断等知识点,侧重考查基本理论,难点是判断原子杂化方式,知道孤电子对个数的计算方法,为易错点,题目难度中等.

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
13.下列有关表述正确的是( )
| A. | 离子晶体一定含金属阳离子 | |
| B. | 非金属元素形成的单质一定是分子晶体 | |
| C. | 在共价化合物分子中各原子都形成8电子结构 | |
| D. | 共价键能存在于共价化合物中,也能存在于离子化合物中 |
14.氯化银在溶液中有极微量的电离:AgCl(s)?Ag+(aq)+Cl-(aq).不能说明该电离达到平衡状态的是( )
| A. | Ag+的浓度不再改变 | |
| B. | Ag+的生成速率和Ag+、Cl-结合生成AgCl的速率相等 | |
| C. | AgCl的质量不再减少 | |
| D. | Ag+与Cl-的物质的量比为1:1 |
11.某原电池反应原理如图所示,下列有关该原电池的说法正确的是( )
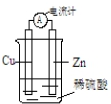

| A. | 电子从锌片经导线流向铜片 | B. | H+向负极移动 | ||
| C. | 一段时间后,铜片质量减轻 | D. | 锌片发生还原反应 |
18.关于有机物说法正确是的( )
| A. | 有机物可分烃和烃的衍生物 | |
| B. | 含C化合物就是有机物 | |
| C. | 有机物都不溶于水,但易溶于有机溶剂 | |
| D. | 有机物都能燃烧 |
7.下列说法不正确的是( )
| A. | 在25℃时,将c mol•L-1的醋酸溶液与0.02mol•L-1NaOH溶液等体积混合后溶液刚好呈中性,用含c的代数式表示CH3COOH的电离常数Ka=$\frac{2×{10}^{-9}}{c-0.02}$ | |
| B. | 0.1 mol•L-1醋酸溶液中:c(H+)2=c (H+)•c(CH3COO-)+KW | |
| C. | 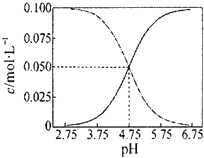 常温下醋酸和醋酸钠混合溶液中c(CH3COOH)、c(CH3COO-)与pH值的关系如图所示,当pH=4.5溶液中:c(CH3COOH)>c(CH3COO-)>c(H+)>c(OH-) | |
| D. | 等体积等物质的量浓度的CH3COONa(aq)与NaCl(aq)中离子总数大小:N前>N后 |
 .
. .
. .
.
 .
.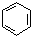 在浓硫酸作用下,与浓硝酸反应的化学方程式为
在浓硫酸作用下,与浓硝酸反应的化学方程式为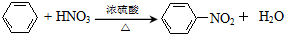 .
.