题目内容
7.在25℃时,有pH=a的盐酸与pH=b的NaOH溶液,取VaL该盐酸同该NaOH溶液恰好反应,需VbLNaOH溶液,问:(1)若a+b=14时,则$\frac{{V}_{a}}{{V}_{b}}$=1(填数值);
(2)若a+b=13时,则$\frac{{V}_{a}}{{V}_{b}}$=0.1(填数值);
(3)若a+b>14时,则$\frac{{V}_{a}}{{V}_{b}}$=10a+b-14(填表达式),且Va>Vb(填>、<或=).
分析 盐酸与氢氧化钠恰好反应,则n(HCl)=n(NaOH),可得Va×10-a=Vb×$\frac{1{0}^{-14}}{1{0}^{-b}}$,整理可得:$\frac{{V}_{a}}{{V}_{b}}$=10a+b-14.
解答 解:盐酸与氢氧化钠恰好反应,则n(HCl)=n(NaOH),可得Va×10-a=Vb×$\frac{1{0}^{-14}}{1{0}^{-b}}$,整理可得:$\frac{{V}_{a}}{{V}_{b}}$=10a+b-14.
(1)若a+b=14时,则$\frac{{V}_{a}}{{V}_{b}}$=10a+b-14=1014-14=1,故答案为:1;
(2)若a+b=13时,则$\frac{{V}_{a}}{{V}_{b}}$=10a+b-14=1013-14=0.1,故答案为:0.1;
(3)若a+b>14时,则$\frac{{V}_{a}}{{V}_{b}}$=10a+b-14>1,则Va>Vb,故答案为:10a+b-14;>.
点评 本题考查溶液pH计算、水电电离平衡等,注意理解掌握强酸与强碱混合呈中性时溶液体积之比规律,侧重考查学生分析计算能力.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
10.化学与工农业生产有密切的联系.下列说法中正确的是( )
| A. | 分子式为(C6H10O5)n的淀粉和纤维素互为同分异构体 | |
| B. | 淀粉、蛋白质、脂肪都是营养物质,都属于高分子化合物 | |
| C. | 在蛋白质溶液中加入饱和硫酸铵溶液,蛋白质析出,虽再加水,也不溶解 | |
| D. | 北京奥运吉祥物“福娃”的材质是PVC(聚氯乙烯),其单体的结构是CH2=CHCl |
7.某电池反应为2Al+6H+=2Al3++3H2↑,下列对该电池推断不正确的是( )
| A. | 铝为负极,镁为正极 | B. | 正极反应式为2H++2e-═H2↑, | ||
| C. | 放电时间越长,溶液中c(H+)越小 | D. | 电解质溶液不可能是硝酸 |
2.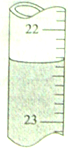 准确移取25.00mL某未知浓度的NaOH溶液于一洁净锥形瓶中,然后用0.20mol/L的盐酸溶液滴定(指示剂为甲基橙),滴定结果如下:
准确移取25.00mL某未知浓度的NaOH溶液于一洁净锥形瓶中,然后用0.20mol/L的盐酸溶液滴定(指示剂为甲基橙),滴定结果如下:
(1)其中第一次滴定达到终点时,滴定管中的液面如上图所示,其正确的读数是22.40mL.
(2)排去酸式滴定管中气泡的具体操作是将酸式滴定管稍稍倾斜,迅速打开活塞,气泡随溶液的流出而被排出;.
(3)根据以上数据可计算出NaOH溶液的物质的量浓度为0.15mol/L.(精确到0.01)
(4)滴定到终点时锥形瓶中溶液的颜色变化是由黄色变为橙色.
(5)下列操作会导致待测NaOH溶液浓度偏高的是AC(填序号).
A.滴定管用蒸馏水洗后未用标准酸液润洗,直接装入标准酸液
B.滴定管读数时,滴定前仰视滴定后俯视
C.滴定前滴定管尖端有气泡,滴后气泡消失
D.滴定到终点附近时,用少量蒸馏水冲洗锥形瓶内壁上沾附的溶液.
 准确移取25.00mL某未知浓度的NaOH溶液于一洁净锥形瓶中,然后用0.20mol/L的盐酸溶液滴定(指示剂为甲基橙),滴定结果如下:
准确移取25.00mL某未知浓度的NaOH溶液于一洁净锥形瓶中,然后用0.20mol/L的盐酸溶液滴定(指示剂为甲基橙),滴定结果如下:| HCl溶液起始读数 | HCl溶液终点读数 | |
| 第一次 | 2.15mL | |
| 第二次 | 3.10mL | 21.85mL |
| 第三次 | 4.20mL | 22.95mL |
(2)排去酸式滴定管中气泡的具体操作是将酸式滴定管稍稍倾斜,迅速打开活塞,气泡随溶液的流出而被排出;.
(3)根据以上数据可计算出NaOH溶液的物质的量浓度为0.15mol/L.(精确到0.01)
(4)滴定到终点时锥形瓶中溶液的颜色变化是由黄色变为橙色.
(5)下列操作会导致待测NaOH溶液浓度偏高的是AC(填序号).
A.滴定管用蒸馏水洗后未用标准酸液润洗,直接装入标准酸液
B.滴定管读数时,滴定前仰视滴定后俯视
C.滴定前滴定管尖端有气泡,滴后气泡消失
D.滴定到终点附近时,用少量蒸馏水冲洗锥形瓶内壁上沾附的溶液.
12.某温度下,硫酸钡与水组成的混合物中,存在下列过程:BaSO4(s)?Ba2++SO42-,向其中加入少量硫酸钠固体,下列说法错误的是( )
| A. | BaSO4的电离程度减小 | B. | BaSO4溶解的量减小 | ||
| C. | c(Ba2+)与c(SO42-)的乘积增大 | D. | 溶液的导电能力增强 |
19. 用O2将HCl转化为Cl2,可提高效益,减少污染,
用O2将HCl转化为Cl2,可提高效益,减少污染,
(1)传统上该转化通过如图所示的催化剂循环实现,其中,反应①为:2HCl(g)+CuO(s)?H2O(g)+CuCl2(g)△H1反应②生成1molCl2(g)的反应热为△H2,则总反应的热化学方程式为2HCl(g)+$\frac{1}{2}$O2(g)?H2O(g)+Cl2(g),△H=(△H1+△H2)kJ/mol,(反应热用△H1和△H2表示).
(2)新型RuO2催化剂对上述HCl转化为Cl2的总反应具有更好的催化活性,
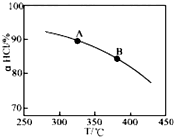
①实验测得在一定压强下,总反应的HCl平衡转化率随温度变化的aHCl-T曲线如图,则总反应的△H<0,(填“>”、“﹦”或“<”);A、B两点的平衡常数K(A)与K(B)中较大的是K(A).
②在上述实验中若压缩体积使压强增大,画出相应aHCl-T(HCl的转化率与温度的关系)曲线的示意图,并简要说明理由: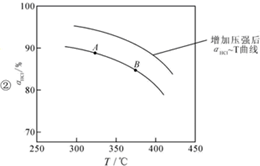 增大压强,平衡右移,ɑHCl增大,相同温度下,HCl的平衡转化率比之前实验的大.
增大压强,平衡右移,ɑHCl增大,相同温度下,HCl的平衡转化率比之前实验的大.
③下列措施中有利于提高aHCl的有BD.
A、增大n(HCl) B、增大n(O2) C、使用更好的催化剂 D、移去H2O
(3)一定条件下测得反应过程中n(Cl2)的数据如下:
计算2.0~6.0min内以HCl的物质的量变化表示的反应速率(以mol•min-1为单位,写出计算过程).
(4)Cl2用途广泛,写出用Cl2制备漂白粉的化学方程式2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
 用O2将HCl转化为Cl2,可提高效益,减少污染,
用O2将HCl转化为Cl2,可提高效益,减少污染,(1)传统上该转化通过如图所示的催化剂循环实现,其中,反应①为:2HCl(g)+CuO(s)?H2O(g)+CuCl2(g)△H1反应②生成1molCl2(g)的反应热为△H2,则总反应的热化学方程式为2HCl(g)+$\frac{1}{2}$O2(g)?H2O(g)+Cl2(g),△H=(△H1+△H2)kJ/mol,(反应热用△H1和△H2表示).
(2)新型RuO2催化剂对上述HCl转化为Cl2的总反应具有更好的催化活性,
①实验测得在一定压强下,总反应的HCl平衡转化率随温度变化的aHCl-T曲线如图,则总反应的△H<0,(填“>”、“﹦”或“<”);A、B两点的平衡常数K(A)与K(B)中较大的是K(A).
②在上述实验中若压缩体积使压强增大,画出相应aHCl-T(HCl的转化率与温度的关系)曲线的示意图,并简要说明理由:
 增大压强,平衡右移,ɑHCl增大,相同温度下,HCl的平衡转化率比之前实验的大.
增大压强,平衡右移,ɑHCl增大,相同温度下,HCl的平衡转化率比之前实验的大.③下列措施中有利于提高aHCl的有BD.
A、增大n(HCl) B、增大n(O2) C、使用更好的催化剂 D、移去H2O
(3)一定条件下测得反应过程中n(Cl2)的数据如下:
| t(min) | 0 | 2.0 | 4.0 | 6.0 | 8.0 |
| n(Cl2)/10-3mol | 0 | 1.8 | 3.7 | 5.4 | 7.2 |
(4)Cl2用途广泛,写出用Cl2制备漂白粉的化学方程式2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O.
16.把0.02mol/L CH3COOH溶液和0.01mol/L NaOH溶液等体积混合,则混合溶液中微粒浓度关系正确的是( )
| A. | (CH3COO-)<c(Na+) | B. | c(CH3COOH)>c(CH3COO-) | ||
| C. | 2c(H+)=c(CH3COO-)-c(CH3COOH) | D. | c(CH3COOH)+c(CH3COO-)=0.01mol/L |
17.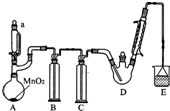 某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验.查阅资料,有关信息如下:
某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验.查阅资料,有关信息如下:
(1)仪器A中发生反应的化学方程式是MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;装置B中的试剂是饱和食盐水.
①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
可能发生的副反应:C2H5OH+HCl→C2H5Cl+H2O
CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相关物质的部分物理性质:
(2)若撤去装置C,可能导致装置D中副产物CCl3COOH、C2H5Cl(填化学式)的量增加;装置D可采用 加热的方法以控制反应温度在70℃左右.
(3)反应结束后,有人提出先将D中的混合物冷却到室温,再用过滤的方法分离出CCl3COOH.你认为此方案是否可行,为什么?不可行,CCl3COOH溶于乙醇与CCl3CHO.
(4)装置E中可能发生的无机反应的离子方程式有Cl2+2OH-=Cl-+ClO-+H2O、H++OH-=H2O.
(5)测定产品纯度:称取产品0.30g配成待测溶液,加入0.1000mol•L-1碘标准溶液20.00mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000mo1•L-1Na2S2O3溶液滴定至终点.进行平行实验后,测得消耗Na2S2O3溶液20.00mL.则产品的纯度为66.4%.(CCl3CHO的相对分子质量为147.5)
滴定的反应原理:CCl3CHO+OH-═CHCl3+HCOO-
HCOO-+I2═H++2I-+CO2↑
I2+2S2O32-═2I-+S4O62-
(6)已知:常温下Ka(CCl3COOH)=1.0×10-1mol•L-1,Ka (CH3COOH)=1.7×10-5mol•L-1
请设计实验证明三氯乙酸、乙酸的酸性强弱.
 某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验.查阅资料,有关信息如下:
某探究小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验.查阅资料,有关信息如下:(1)仪器A中发生反应的化学方程式是MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O;装置B中的试剂是饱和食盐水.
①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
可能发生的副反应:C2H5OH+HCl→C2H5Cl+H2O
CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相关物质的部分物理性质:
| C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
| 熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
| 沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
| 溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇 | 微溶于水、可溶于乙醇 |
(3)反应结束后,有人提出先将D中的混合物冷却到室温,再用过滤的方法分离出CCl3COOH.你认为此方案是否可行,为什么?不可行,CCl3COOH溶于乙醇与CCl3CHO.
(4)装置E中可能发生的无机反应的离子方程式有Cl2+2OH-=Cl-+ClO-+H2O、H++OH-=H2O.
(5)测定产品纯度:称取产品0.30g配成待测溶液,加入0.1000mol•L-1碘标准溶液20.00mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000mo1•L-1Na2S2O3溶液滴定至终点.进行平行实验后,测得消耗Na2S2O3溶液20.00mL.则产品的纯度为66.4%.(CCl3CHO的相对分子质量为147.5)
滴定的反应原理:CCl3CHO+OH-═CHCl3+HCOO-
HCOO-+I2═H++2I-+CO2↑
I2+2S2O32-═2I-+S4O62-
(6)已知:常温下Ka(CCl3COOH)=1.0×10-1mol•L-1,Ka (CH3COOH)=1.7×10-5mol•L-1
请设计实验证明三氯乙酸、乙酸的酸性强弱.