题目内容
下列说法中正确的是( )
| A、CH3CH2OH、SO3和水分别属于非电解质、强电解质和弱电解质 |
| B、为测定熔融氢氧化钠的导电性,可将氢氧化钠固体放在石英坩埚中加热熔化 |
| C、煤油可由石油分馏获得,可用于保存少量金属钠 |
| D、工业上金属Mg、Al都是用电解其相应的氯化物水溶液制得的 |
考点:强电解质和弱电解质的概念,硅和二氧化硅,金属冶炼的一般原理,钠的化学性质
专题:电离平衡与溶液的pH专题,碳族元素,几种重要的金属及其化合物
分析:A、SO3在水溶液和熔融状态下不能发生电离,是非电解质;
B、氢氧化钠可与二氧化硅反应;
C、煤油是石油分馏的产品,金属钠性质活泼,能与氧气、水发生反应,煤油可以隔绝氧气、水;
D、氢离子的氧化性大于镁离子、铝离子,工业制Mg、Al是分别电解熔融MgCl2和Al2O3来制取.
B、氢氧化钠可与二氧化硅反应;
C、煤油是石油分馏的产品,金属钠性质活泼,能与氧气、水发生反应,煤油可以隔绝氧气、水;
D、氢离子的氧化性大于镁离子、铝离子,工业制Mg、Al是分别电解熔融MgCl2和Al2O3来制取.
解答:
解:A、SO3在水溶液或熔融状态下不能发生电离,是非电解质,故A错误;
B、瓷坩埚的主要成分是二氧化硅,加热条件下二氧化硅可与氢氧化钠反应生成硅酸钠,导致坩埚炸裂,故B错误;
C、煤油是石油分馏的产品,金属钠性质活泼,能与氧气、水发生反应,煤油可以隔绝氧气、水,因此少量的金属钠可以保存在煤油中,故C正确;
D、工业制Mg是电解熔融氯化镁,工业制铝是电解熔融的氧化铝:2Al2O3
4Al+3O2↑,氢离子的氧化性大于镁离子、铝离子,不是电解氯化物的水溶液,故D错误;
故选C.
B、瓷坩埚的主要成分是二氧化硅,加热条件下二氧化硅可与氢氧化钠反应生成硅酸钠,导致坩埚炸裂,故B错误;
C、煤油是石油分馏的产品,金属钠性质活泼,能与氧气、水发生反应,煤油可以隔绝氧气、水,因此少量的金属钠可以保存在煤油中,故C正确;
D、工业制Mg是电解熔融氯化镁,工业制铝是电解熔融的氧化铝:2Al2O3
| ||
| 冰晶石 |
故选C.
点评:本题考查较为综合,涉及电解质、非电解质、强电解质和弱电解质的概念、金属的冶炼、二氧化硅的性质等知识,为高频考点,注意把握物质的性质是关键,注意相关基础知识的学习,难度不大.

练习册系列答案
相关题目
下列离子在给定的条件下一定能大量共存的是( )
| A、加入Al粉放出H2的溶液中:Na+、K+、Fe3+、NO3- |
| B、c(Fe3+)=0.1mol/L的溶液中:NH4+、AlO2-、SO42-、HCO3- |
| C、水电离出的c(H+)=1×10-13mol/L的溶液中:Mg2+、K+、NO3-、Cl- |
| D、c(H+)=1×10-13mol/L的溶液中:K+、Cl-、AlO2-、CO3- |
下列说法正确的是( )
| A、摩尔是7个基本物理量之一 |
| B、18 g水在标准状况下的体积约为22.4 L |
| C、27 g Al约含有6.02×1023个铝原子 |
| D、配制0.1 mol/L的NaCl溶液需NaCl固体的质量为5.85 g |
短周期主族元素X、Y、Z、W,原子序数依次增大.X、Z同主族,X、Y、Z三种元素主族序数之和为15,Y原子最外层电子数等于X原子最外层电子数的一半.下列叙述正确的是( )
| A、非金属性:X<Z |
| B、原子半径:X<W<Z<Y |
| C、最高价氧化物对应水化物的酸性:W<Z |
| D、单质Y常温下能溶于浓硝酸 |
关于容量瓶的叙述:①是配制准确物质的量浓度溶液的仪器;②不宜长时间贮存溶液;③能用来加热;④使用之前要检查是否漏水.这些叙述中正确的有( )
| A、①②③④ | B、②③ |
| C、①②④ | D、②③④ |
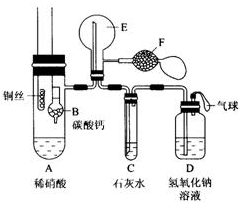 为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去).B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为 一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.
为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去).B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为 一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.