题目内容
下列说法或表示方法正确的是( )
| A、等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 |
| B、由C(金刚石,s)═C(石墨,s)△H=-1.90 kJ?mol-1可知,金刚石比石墨稳定 |
| C、在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=285.8 kJ?mol-1 |
| D、稀溶液中H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ?mol-1若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、等质量的硫蒸气具有的能量比硫固体多;
B、根据能量越低越稳定判断;
C、2g氢气是1mol;
D、浓硫酸溶于水放热;
B、根据能量越低越稳定判断;
C、2g氢气是1mol;
D、浓硫酸溶于水放热;
解答:
解:A、等质量的硫蒸气和硫固体相比较,硫蒸气具有的能量多,因此完全燃烧硫蒸气放出的热量多,故A错误;
B、C(石墨)=C(金刚石)△H=+1.90 kJ/mol可知石墨能量比金刚石低,石墨较稳定,故B错误;
C、2g氢气是1mol,1mol氢气燃烧放热285.8KJ,氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol,故C错误;
D、浓硫酸溶于水放热,则将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,生成1mol水,放出的热大于57.3 kJ,故D正确;
故选D.
B、C(石墨)=C(金刚石)△H=+1.90 kJ/mol可知石墨能量比金刚石低,石墨较稳定,故B错误;
C、2g氢气是1mol,1mol氢气燃烧放热285.8KJ,氢气燃烧的热化学方程式为:2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ/mol,故C错误;
D、浓硫酸溶于水放热,则将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,生成1mol水,放出的热大于57.3 kJ,故D正确;
故选D.
点评:本题考查了物质状态本题所含能量不同、物质的能量越低越稳定、中和热的相关知识,题目难度不大.

练习册系列答案
相关题目
下列关于物质的分离、提纯实验中的一些操作或做法,其中不正确的是( )
| A、在组装蒸馏装置时,温度计的水银球应伸入液面下 |
| B、用96%的工业酒精制取无水乙醇,可采用的方法是加生石灰,再蒸馏 |
| C、在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还要加少量蒸馏水 |
| D、分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 |
NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、125g CuSO4?5H2O晶体中含有Cu2+离子数小于0.5NA |
| B、7.8 g Na2S和Na2O2的混合物中含有的阴离子数大于0.1NA |
| C、由S4、S6、S8组成的硫蒸气6.4 g,其中所含硫原子数一定为0.2NA |
| D、3.6 gC与3.36LO2一定条件下恰好完全反应,生成CO分子数一定为0.3NA |
下列关于物质的性质与应用相对应的是( )
| A、氯气有毒,不可用作自来水的杀菌消毒 |
| B、FeCl3溶液能与Cu反应,可用于蚀刻印刷电路 |
| C、硫粉具有还原性,可用于制造黑火药 |
| D、Na2O2具有强氧化性,可用作呼吸面具的供氧剂 |
下列有机物中,属于高分子化合物的是( )
| A、油脂 | B、淀粉 | C、葡萄糖 | D、果糖 |
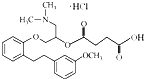 ),是改善慢性动脉闭塞症所引起的溃疡、疼痛以及冷感等缺血性诸症状的一种药物.其合成路线如下:
),是改善慢性动脉闭塞症所引起的溃疡、疼痛以及冷感等缺血性诸症状的一种药物.其合成路线如下: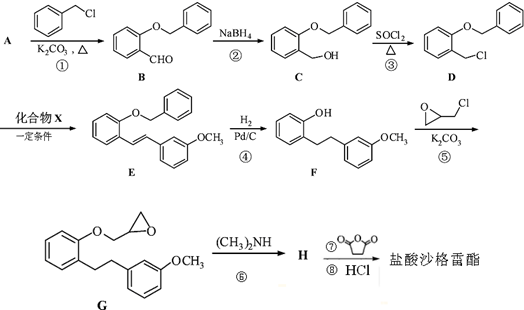
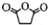 是丁二酸酐
是丁二酸酐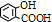 ),分析该制备过程的关键所在
),分析该制备过程的关键所在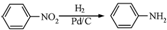 .化合物
.化合物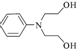 是合成抗癌药物的中间体,请写出以
是合成抗癌药物的中间体,请写出以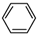 和
和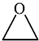 为原料制备该化合物的合成路线流程图(无机试剂任用).
为原料制备该化合物的合成路线流程图(无机试剂任用).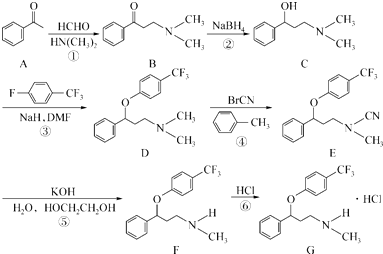
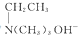
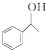 、HCHO、CH3I、HN(CH3)2为有机原料,合成
、HCHO、CH3I、HN(CH3)2为有机原料,合成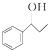 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:


