题目内容
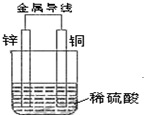 根据如图填空(涉及到电极填写具体物质的元素符号)
根据如图填空(涉及到电极填写具体物质的元素符号)(1)电子流向从
(2)H+向
(3)负极电极反应式
考点:原电池和电解池的工作原理
专题:电化学专题
分析:该装置是原电池,Zn易失电子为负极、Cu为正极,负极反应式为Zn-2e-=Zn2+、2H++2e-=H2↑,电子从负极沿导线流向正极,电解质溶液中阳离子向正极移动、阴离子向负极移动,据此分析解答.
解答:
解:(1)该装置是原电池,Zn易失电子作负极、Cu作正极,电子从负极Zn沿导线流向正极Cu,故答案为:Zn;Cu;
(2)电解质溶液中氢离子向正极Cu移动,正极上电极反应式为2H++2e-=H2↑,所以溶液中氢离子浓度降低,溶液的pH升高,故答案为:Cu;变大;
(3)负极反应式为Zn-2e-=Zn2+,失电子发生氧化反应,
故答案为:Zn-2e-=Zn2+;氧化.
(2)电解质溶液中氢离子向正极Cu移动,正极上电极反应式为2H++2e-=H2↑,所以溶液中氢离子浓度降低,溶液的pH升高,故答案为:Cu;变大;
(3)负极反应式为Zn-2e-=Zn2+,失电子发生氧化反应,
故答案为:Zn-2e-=Zn2+;氧化.
点评:本题考查原电池原理,侧重考查电极反应式书写、电子流向及阴阳离子移动方向等知识点,电解质溶液中阴阳离子移动方向是学习难点,题目难度不大.

练习册系列答案
相关题目
将一定量的NaHCO3和Na2O2的混合物置于一密闭容器中充分加热,反应中转移的电子数为1mol,下列说法一定正确的是( )
| A、混合物中NaHCO3和Na2O2物质的量一定相等 |
| B、容器中肯定有0.5molO2 |
| C、反应后,容器中的固体只有Na2CO3 |
| D、反应后,容器中一定没有H2O |
书写热化学方程式要注明物质的聚集状态,原因是( )
| A、具体说明反应的情况 |
| B、说明反应条件 |
| C、物质呈现的状态与反应焓变有关 |
| D、物质呈现的状态与生成什么物质有关 |
已知草酸钠与高锰酸钾反应的化学方程式为:5Na2C2O4+2KMnO4+8H2SO4═l0CO2↑+2MnSO4+K2SO4+8H2O+5Na2SO4.下列有关说法中正确的是( )
| A、H2SO4含有离子键和共价键 |
| B、Na2C2O4被还原 |
| C、标准状况下,每转移l mol电子生成11.2L的混合气体 |
| D、CO2只含极性键 |
下列关于乙醇的说法正确的是( )
| A、用萃取分液的方法除去酒精中的水 |
| B、可由乙烯通过加成反应制取 |
| C、也可用来保存金属钠 |
| D、无水乙醇常用于医疗消毒 |
设NA为阿伏加德罗常数,则下列说法正确的是( )
| A、一定条件下,2.3gNa完全与O2反应生成3.6g产物时得到的电子数为0.1NA |
| B、1L0.1mol/L醋酸溶液中所含分子数少于0.1NA |
| C、1mol羟基中含有的电子总数为9NA |
| D、1molH2O2含有极性共价键键数为NA,含有非极性共价键为键数2NA |
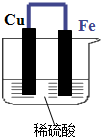 如图示的装置中
如图示的装置中