题目内容
下表是周期表中的一部分,根据A-N在周期表中的位置,按要求回答下列问题:
(1)表中元素,只有负价而无正价的元素是 ,还原性最强的单质是 ;(用相关的元素符号或分子式表示)
(2)表中元素,最高价氧化物的水化物碱性最强的是 ,酸性最强的是 ,呈两性的是 ;(用相关化学式表示)
(3)A、B、C、F形成的单质中,熔点最高的物质的名称为 .
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I | J | K | M | N |
(2)表中元素,最高价氧化物的水化物碱性最强的是
(3)A、B、C、F形成的单质中,熔点最高的物质的名称为
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表中位置,可知A为氢、B为碳、C为氮、D为氟、E为He、F为Na、G为Mg、H为Al、I为Si、J为磷、K为硫、M为Cl、N为Ar.
(1)F元素只有负化合价,没有正化合价;同周期自左而右金属性减弱,同主族自上而下金属性增强,金属性越强,还原性越强;
(2)上述元素中Na的金属性最强,故氢氧化钠碱性最强,高氯酸的酸性最强,氢氧化铝是两性氢氧化物;
(3)根据晶体类型及常温下物质的状态判断熔点.
(1)F元素只有负化合价,没有正化合价;同周期自左而右金属性减弱,同主族自上而下金属性增强,金属性越强,还原性越强;
(2)上述元素中Na的金属性最强,故氢氧化钠碱性最强,高氯酸的酸性最强,氢氧化铝是两性氢氧化物;
(3)根据晶体类型及常温下物质的状态判断熔点.
解答:
解:由元素在周期表中位置,可知A为氢、B为碳、C为氮、D为氟、E为He、F为Na、G为Mg、H为Al、I为Si、J为磷、K为硫、M为Cl、N为Ar.
(1)F元素只有负化合价,没有正化合价;上述元素中Na的金属性最强,金属性越强,还原性越强,故Na的还原性最强,故答案为:F;Na;
(2)上述元素中Na的金属性最强,故NaOH碱性最强,HClO4的酸性最强,Al(OH)3是两性氢氧化物,
故答案为:NaOH;HClO4;Al(OH)3;
(3)A单质为氢气,C的单质为氮气,二者常温下为气体,F的单质为金属晶体,但B的单质中金刚石为原子晶体,熔点最高,
故答案为:金刚石.
(1)F元素只有负化合价,没有正化合价;上述元素中Na的金属性最强,金属性越强,还原性越强,故Na的还原性最强,故答案为:F;Na;
(2)上述元素中Na的金属性最强,故NaOH碱性最强,HClO4的酸性最强,Al(OH)3是两性氢氧化物,
故答案为:NaOH;HClO4;Al(OH)3;
(3)A单质为氢气,C的单质为氮气,二者常温下为气体,F的单质为金属晶体,但B的单质中金刚石为原子晶体,熔点最高,
故答案为:金刚石.
点评:本题考查元素周期表与元素周期律,比较基础,侧重对基础知识的巩固.

练习册系列答案
相关题目
下列各组中互为同位素的是( )
| A、重氢、超重氢 |
| B、氧气、臭氧 |
| C、金刚石、石墨 |
| D、水、重水 |
若在加入铝粉能放出H2的溶液中,下列各组离子一定不能大量共存的是( )
| A、Na+、Fe3+、SO42-、Cl- |
| B、Ba2+、Mg2+、HCO3-、Cl- |
| C、Na+、K+、NO3-、CO32- |
| D、K+、NO3-、AlO2-、OH- |
50mL BaCl2溶液所含有的Cl-,与20mL 0.5mol?L-1的硝酸银溶液恰好完全反应,则原溶液BaCl2的物质的量的浓度是( )
| A、1 mol?L-1 |
| B、0.8 mol?L-1 |
| C、0.2 mol?L-1 |
| D、0.1 mol?L-1 |
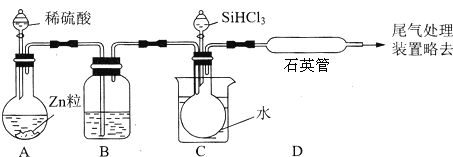
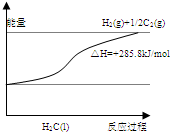 A、B、C、D、E是原子序数依次增大的前四周期元素,其信息如表:
A、B、C、D、E是原子序数依次增大的前四周期元素,其信息如表: