题目内容
取100ml的食盐水用惰性电极进行电解,当阳极析出11.2L气体(标准状况)时,食盐恰好完全电解,试计算:
(1)所取食盐水中氯化钠的物质的量浓度是________;流经导线的电子数目________
(2)要使溶液恢复到原状态,需加入的是物质________,其质量是________。
10mol/L NA 氯化氢 36.5g
考查电化学的有关计算。
(1)惰性电极电解饱和食盐水,阳极是氯离子失去电子生成氯气,电极反应式是2Cl--2e-=Cl2↑,氯气的物质的量是11.2L÷22.4L/mol=0.5mol
所以根据原子守恒可知,氯化钠的物质的量就是1.0mol
其浓度是1.0mol÷0.1L=10mol/L
流经导线的电子数目是0.5×2×NA=NA。
(2)应用阴极是氢离子得到电子,生成氢气,根据电子的得失守恒可知,氢气也是0.5mol。所以要使溶液恢复到原状态,需加入的物质是1.0mol氯化氢,质量是1mol×36.5g/mol=36.5g。
考查电化学的有关计算。
(1)惰性电极电解饱和食盐水,阳极是氯离子失去电子生成氯气,电极反应式是2Cl--2e-=Cl2↑,氯气的物质的量是11.2L÷22.4L/mol=0.5mol
所以根据原子守恒可知,氯化钠的物质的量就是1.0mol
其浓度是1.0mol÷0.1L=10mol/L
流经导线的电子数目是0.5×2×NA=NA。
(2)应用阴极是氢离子得到电子,生成氢气,根据电子的得失守恒可知,氢气也是0.5mol。所以要使溶液恢复到原状态,需加入的物质是1.0mol氯化氢,质量是1mol×36.5g/mol=36.5g。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
(8分)(1)在实验室中,下列实验中所选用的仪器或操作合理的是_____________
| A.用200mL量筒量取5.25mL稀H2SO4 |
| B.用托盘天平称取11.7gNaCl晶体 |
| C.用100mL烧杯配制50g质量分数约为1%的食盐水 |
| D.用500mL容量瓶配制250mL0.20mol/L的氢氧化钠溶液 |
F.盛装Ca(OH)2溶液的试剂瓶可用玻璃塞
G.萃取分液时,先将上层液小心从上口倒出,再将下层液从下口流出
H.蒸馏时,温度计水银球放入液面以下,但不可触及瓶底或沸石
(2)乙醇(俗名酒精)的结构简式为CH3CH2OH,其分子式为C2H6O,相对分子质量为______________,摩尔质量为_____________

 。
。
 )。饮用水中ClO2、
)。饮用水中ClO2、
 ,则步骤4中加入的指示剂为_________,滴定达到终点时溶液的颜色变化为___________________________。
,则步骤4中加入的指示剂为_________,滴定达到终点时溶液的颜色变化为___________________________。 将溶液中的
将溶液中的 还原为
还原为 以测定其含量,该反应的离子方程式为_________________
_____________。
以测定其含量,该反应的离子方程式为_________________
_____________。


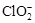 )。饮用水中ClO2、
)。饮用水中ClO2、
 ,则步骤4中加入的指示剂为
,滴定达到终点时溶液的颜色变化为
,则步骤4中加入的指示剂为
,滴定达到终点时溶液的颜色变化为
 将溶液中的
将溶液中的 还原为
还原为 以测定其含量,该反应的离子方程式为:
以测定其含量,该反应的离子方程式为: 将
将