题目内容
8.某温度时,BaCO3在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )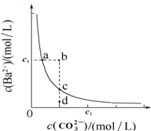
| A. | 通过蒸发可以使溶液由d点变到c点 | |
| B. | b点有BaCO3沉淀生成 | |
| C. | 升高温度,可以使d点变为c点 | |
| D. | 在a点加入Na2CO3,达平衡时c(Ba2+)≠c(CO32-),其Ksp大于c点对应的Ksp |
分析 A.蒸发时c(Ba2+)、c(CO32-)均增大;
B.b点时Qc(BaCO3)=c(Ba2+)×c(CO32-)>Ksp(BaCO3);
C.升高温度时BaCO3?Ba2++CO32-正向移动,c(Ba2+)、c(CO32-)均增大;
D.Ksp只与温度有关.
解答 解:A.蒸发时c(Ba2+)、c(CO32-)均增大,d点变到c点时c(CO32-)不变,则蒸发不能实现,故A错误;
B.b点时Qc(BaCO3)=c(Ba2+)×c(CO32-)>Ksp(BaCO3),则b点有BaCO3沉淀生成,故B正确;
C.升高温度时BaCO3?Ba2++CO32-正向移动,c(Ba2+)、c(CO32-)均增大,d点变到c点时c(CO32-)不变,则升高温度不能使d点变为c点,故C错误;
D.Ksp只与温度有关,则在a点加入Na2CO3,达平衡时c(Ba2+)≠c(CO32-),其Ksp等于c点对应的Ksp,故D错误;
故选B.
点评 本题考查难溶电解质的溶解平衡,为高频考点,把握图中离子浓度变化、溶解平衡移动为解答的关键,侧重分析与应用能力的考查,注意Ksp只与温度有关,题目难度不大.

练习册系列答案
相关题目
13.下列实验的操作和所用的试剂都正确的是( )
| A. | 要检验己烯中是否混有少量甲苯,应先加足量溴水,然后再加入酸性高锰酸钾溶液 | |
| B. | 配制浓硫酸和浓硝酸的混酸时,将浓硝酸沿壁缓缓倒入到浓硫酸中 | |
| C. | 制硝基苯时,将盛有混合液的试管直接在酒精灯火焰上加热 | |
| D. | 除去乙酸乙酯中少量的乙酸,可以加氢氧化钠溶液后分液 |
11.同温、同压下,盛有氧气的A容器与盛有氨气的B容器中,所含原子个数相等,则A与B的体积比是( )
| A. | 1:1 | B. | 2:1 | C. | 1:2 | D. | 2:3 |
3.甲、乙、丙、丁四种有机物的结构如表:
球棍模型中“棍”代表单键或双键或三键.
下列叙述不正确的是( )
| 甲的球棍模型 | 乙的结构式 | 丙的球棍模型 | 丁的比例模型 |
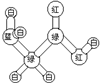 | 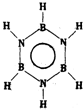 | 丙的分子式为C13H10O3 | 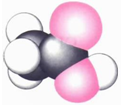 |
下列叙述不正确的是( )
| A. | 甲可代表氨基酸 | B. | 乙的二氯代物有3种 | ||
| C. | 丙的结构简式为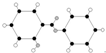 | D. | 丁可代表乙酸 |
20.下列物质燃烧时,不会造成大气污染的是( )
| A. | 石油 | B. | 农作物秸秆 | C. | 煤 | D. | 氢气 |
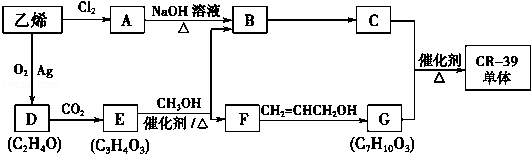
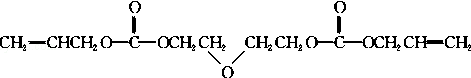
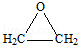 .
.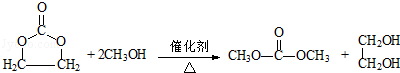 .
.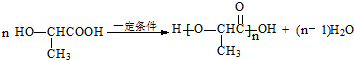 .
.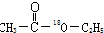 的合成路线,合成路线流程图示例如下:CH2-CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.
的合成路线,合成路线流程图示例如下:CH2-CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH.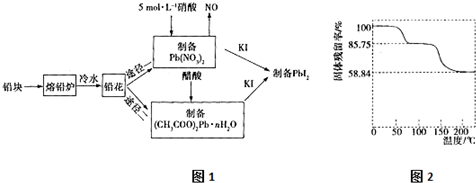
 .
.