题目内容
 高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂.其水溶液中FeO
高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂.其水溶液中FeO2- 4 |
| A、不论溶液酸碱性如何变化,铁元素都有4种存在形态 |
| B、向pH=2的这种溶液中加KOH溶液至pH=10,HFeO4-的分布分数先减小后增大 |
| C、pH=2的这种溶液中存在如下等式关系:2[K+]=[H3FeO4+]+[H2FeO4]+[HFeO4-] |
| D、pH=8的这种溶液中存在如下等式关系:[K+]+[H+]=[OH-]+[HFeO4-]+2[FeO42-] |
考点:离子浓度大小的比较,氧化还原反应,盐类水解的应用
专题:基本概念与基本理论
分析:A.pH不同,铁元素的存在种类不同;
B.根据不同pH时,HFeO4-的变化图象判断;
C.任何电解质溶液中都存在物料守恒,根据物料守恒判断;
D.任何电解质溶液中都存在电荷守恒,根据电荷守恒判断.
B.根据不同pH时,HFeO4-的变化图象判断;
C.任何电解质溶液中都存在物料守恒,根据物料守恒判断;
D.任何电解质溶液中都存在电荷守恒,根据电荷守恒判断.
解答:
解:A.pH不同,铁元素存在的种类不同,如pH=8时Fe元素有两种微粒,故A错误;
B.pH由2变化为10时,HFeO4-的分布分数先增大后减小,故B错误;
C.任何电解质溶液中都存在物料守恒,根据物料守恒得[K+]=2[H3FeO4+]+2[H2FeO4]+2[HFeO4-],故C错误;
D.任何电解质溶液中都存在电荷守恒,根据电荷守恒得:[K+]+[H+]=[OH-]+[HFeO4-]+2[FeO42-],故D正确;
故选D.
B.pH由2变化为10时,HFeO4-的分布分数先增大后减小,故B错误;
C.任何电解质溶液中都存在物料守恒,根据物料守恒得[K+]=2[H3FeO4+]+2[H2FeO4]+2[HFeO4-],故C错误;
D.任何电解质溶液中都存在电荷守恒,根据电荷守恒得:[K+]+[H+]=[OH-]+[HFeO4-]+2[FeO42-],故D正确;
故选D.
点评:本题以盐类水解为载体考查了离子浓度大小比较,明确图象中曲线变化趋势是解本题关键,再结合守恒思想分析解答,题目难度不大.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
三氧化二镍(Ni2O3)可用于制造高能电池,其电解法制备过程如下:用NaOH调NiCl2溶液pH至7.5,加放适量硫酸钠后进行电解.电解过程中产生的Cl2在弱碱性条件下生成ClO-,把二价镍氧化为三价镍.以下说法不正确的是( )
| A、可用铁作阳极材料 |
| B、电解过程中阳极附近溶液的pH降低 |
| C、阳极反应方程式为:2Cl--2e-═Cl2 |
| D、1 mol二价镍全部转化为三价镍时,外电路中通过了1 mol电子 |
为了除去NO、NO2、NO2O4对大气的污染,常采用氢氧化钠溶液进行吸收处理反应方程式:2NO2+2NaOH→NaNO3+NaNO2+H2O;NO2+NO+2NaOH→2NaNO2+H2O.现有由a mol NO、b mol NO2、c mol N2O4组成的混合气体恰好被V L氢氧化钠溶液吸收(无气体剩余).这次氢氧化钠溶液的物质的量浓度最小为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
aA、bB、cC、dD、eE均为短周期元素.已知D与E同主族,其中d=
,c-l=
,c-d=
.下列说法正确的是( )
| e |
| 2 |
| d+e |
| 2 |
| b-a |
| 2 |
| A、原子半径:E>D>C |
| B、元素A与B一定同主族,且B为第3周期元素 |
| C、元素C的最高价氧化物属于碱性氧化物 |
| D、元素E的常见氧化物有2种,且它们之间可以相互转化 |
能正确表示下列反应的离子方程式是( )
| A、少量的CO2通人氨水中:CO2+NH3?H2O═NH4++HCO3- | ||||
| B、Na2O2溶于水中:2Na2O2+2H2O═4Na++4OH-+O2↑ | ||||
| C、钢铁发生吸氧腐蚀时,铁作负极被氧化:Fe-3e-═Fe3+ | ||||
D、用惰性电极电解熔融氯化钠:2Cl-+2H2O
|
下列说法正确的是( )
| A、向Na2CO3溶液中滴入酚酞后溶液变成红色,说明Na2CO3溶液具有碱性,属于碱 |
| B、将SO2通入氯水中,溶液颜色退去,说明SO2具有漂白性 |
| C、制备无水AlCl3、FeCl3、CuCl2均不能采用将溶液直接蒸干的方法 |
| D、Fe与稀硝酸、稀硫酸反应均有气泡冒出,说明Fe与两种酸均发生了置换反应 |
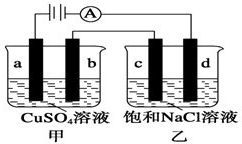 如图a、b、c、d均为石墨电极,通电进行电解(电解液足量).下列说法不正确的是( )
如图a、b、c、d均为石墨电极,通电进行电解(电解液足量).下列说法不正确的是( )| A、甲中a的电极反应式为4OH--4e-═O2↑+2H2O |
| B、向乙中加入适量盐酸,溶液组成可以恢复 |
| C、电解时向乙中滴入酚酞溶液,d电极附近先变红 |
| D、当b极有6.4g Cu析出时,c电极产生7.1g气体 |
下列关于金属腐蚀的叙述不正确的是( )
A、金属在潮湿情况下的腐蚀实质是M+nH2O=M(OH)n+
| ||
| B、金属的化学腐蚀实质是M-ne-=Mn+,电子直接转移给氧化剂 | ||
| C、在潮湿的中性环境中,金属的电化学腐蚀主要是吸氧腐蚀 | ||
| D、防止金属发生电化学腐蚀,关键在于阻止金属成为原电池的负极,避免其发生阳极氧化而溶解. |