题目内容
向三份0.1mol/LCH3COONa溶液中分别加入少量NH4NO3、Na2SO3、FeCl2因体(忽略溶液体积变化,( CH3COO)2Fe为易溶于水的盐且完全电离),则CH3COO-浓度的变化依次为( )
| A、减小、增大、减小 |
| B、增大、减小、减小 |
| C、减小、增大、增大 |
| D、增大、减小、增大 |
考点:影响盐类水解程度的主要因素
专题:
分析:含有弱根离子的盐溶液,如果两种溶液的酸碱性相同,那么它们混合后会相互抑制水解;如果一种溶液显酸性,另一种溶液显碱性,那么它们混合后弱根离子能相互促进水解.
解答:
解:含有弱根离子的盐溶液,如果两种溶液的酸碱性相同,那么它们混合后会相互抑制水解;如果一种溶液显酸性,另一种溶液显碱性,那么它们混合后弱根离子能相互促进水解.
醋酸钠是强碱弱酸盐其水溶液呈碱性,硝酸铵是强酸弱碱盐其水溶液呈酸性,所以向醋酸钠溶液中加硝酸铵会促进醋酸根离子水解,导致醋酸根离子浓度减小;
亚硫酸钠是强碱弱酸盐其水溶液呈碱性,所以向醋酸钠溶液中加亚硫酸钠会抑制醋酸根离子的水解,导致醋酸根离子浓度增大;
氯化铁是强酸弱碱盐其水溶液呈酸性,所以向醋酸钠溶液中加氯化铁会促进醋酸根离子水解,导致醋酸根离子浓度减小,
故选A.
醋酸钠是强碱弱酸盐其水溶液呈碱性,硝酸铵是强酸弱碱盐其水溶液呈酸性,所以向醋酸钠溶液中加硝酸铵会促进醋酸根离子水解,导致醋酸根离子浓度减小;
亚硫酸钠是强碱弱酸盐其水溶液呈碱性,所以向醋酸钠溶液中加亚硫酸钠会抑制醋酸根离子的水解,导致醋酸根离子浓度增大;
氯化铁是强酸弱碱盐其水溶液呈酸性,所以向醋酸钠溶液中加氯化铁会促进醋酸根离子水解,导致醋酸根离子浓度减小,
故选A.
点评:本题考查了影响盐类水解的因素,明确含有弱根离子的盐溶液,如果两种溶液的酸碱性相同,那么它们混合后会相互抑制水解;如果一种溶液显酸性,另一种溶液显碱性,那么它们混合后弱根离子能相互促进水解.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A、1 mol NaHSO4固体中含离子总数为3NA |
| B、标准状况下,11.2 L SO3中含有分子的数目为0.5NA |
| C、1 mol FeI2与足量氯气反应时转移的电子数为3NA |
| D、1.6 g由氧气和臭氧组成的混合物中含有分子的数目为0.1NA |
下列物质必须保存在棕色试剂瓶中的是( )
①氯水 ②氨水 ③浓硝酸 ④氢氧化钠 ⑤溴水.
①氯水 ②氨水 ③浓硝酸 ④氢氧化钠 ⑤溴水.
| A、全部 | B、①③⑤ |
| C、①②③ | D、①②④ |
下列各组物质的转化关系中不能全部是通过一步反应完成的是( )
| A、Na→NaOH→Na2CO3→NaCl |
| B、Fe→Fe(NO3)3→Fe(OH)3→Fe2O3 |
| C、Mg→MgCl2→Mg(OH)2→MgSO4 |
| D、Si→SiO2→H2SiO3→Na2SiO3 |
下列关于氯水的叙述错误的是( )
| A、新制氯水中只含Cl2和H2O分子 |
| B、光照氯水有气泡放出,该气体是O2 |
| C、氯水放置一段时间后颜色将变浅 |
| D、新制氯水可使紫色石蕊试液先变红后褪色 |
航天飞机用高氯酸铵(NH4ClO4)与铝粉的混合物为固体燃料,点燃时铝粉氧化放热引发高氯酸铵反应,方程式为:2NH4ClO4(s)N
2(g)+4H2O(g)+Cl2(g)+2O2(g)△H=-Q kJ/mol下列不正确的是( )
| ||
| A、上述反应属于分解反应 |
| B、上述反应瞬间产生大量高温气体推动航天飞机飞行 |
| C、反应从能量变化上看,主要是化学能转变为热能和动能 |
| D、在反应中高氯酸铵只起氧化剂的作用 |
现有CO、CO2和O3三种气体,它们都含有1摩尔氧原子,则三种气体的物质的量之比为( )
| A、1:1:1: |
| B、1:2:3 |
| C、3:2:1 |
| D、6:3:2 |
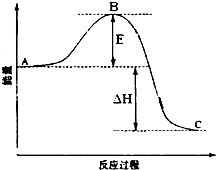 2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3放出的热量99kJ.请回答下列问题:
2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3放出的热量99kJ.请回答下列问题: