题目内容
18.5molCO2的质量是220g;在标准状况下所占的体积约为112L;所含氧原子的数目为6.02×1024个.分析 根据m=nM计算二氧化碳质量,根据V=nVm计算其体积,氧原子物质的量为二氧化碳的2倍,再根据N=nNA计算氧原子数目.
解答 解:5molCO2的质量是5mol×44g/mol=220g,在标准状况下所占的体积约为5mol×22.4L/mol=112 L,所含氧原子的数目为5mol×2×6.02×1023mol-1=6.02×1024,
故答案为:220;112;6.02×1024.
点评 本题考查物质的量有关计算,比较基础,注意掌握以物质的量为中心的计算公式.

练习册系列答案
相关题目
8.在下列各组离子在指定溶液中,一定能大量共存的是( )
| A. | 室温下,pH=1的溶液中:Na+、Fe3+、NO3-、I- | |
| B. | 水电离的H+浓度为1×10-13mol•L-1的溶液中,K+、Al3+、Cl-、SO42- | |
| C. | AlO2?浓度为0.1 mol•L-1的溶液中:Na+、K+、HCO3-、Cl- | |
| D. | 加入KSCN溶液显红色的溶液:K+、NH4+、Cl-、NO3- |
9.下列说法正确的是( )
| A. | 标准状况下,1mol H2完全燃烧生成气态水放出285.8kJ热量,则H2的燃烧热为-285.8kJ•mol-1 | |
| B. | 测定HCl和NaOH反应的中和热时,每次实验均应测量3个温度,即盐酸起始温度,NaOH起始温度和反应后最高温度 | |
| C. | 在101 kPa时,1mol C与适量O2反应生成1mol CO时,放出110.5kJ热量,则C的燃烧热为110.5kJ•mol-1 | |
| D. | 在稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.31 kJ•mol-1.若将含0.5mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量等于57.3kJ |
6.下列有关物质用途的说法中,不正确的是( )
| A. | 液氨可做致冷剂 | |
| B. | 二氧化硅可作为半导体材料 | |
| C. | 氢氧化铝常用于中和胃酸 | |
| D. | 常温下,铁制容器常用于盛装浓硫酸 |
13.如图各情况,在其中Fe片腐蚀由快到慢的顺序是( )
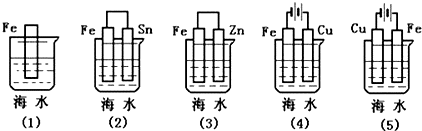

| A. | (5)(2)(1)(3)(4) | B. | (5)(2)(3)(1)(4) | C. | (4)(2)(1)(3)(5) | D. | (4)(2)(1)(5)(3) |
3.下列各种冶炼方法中,可制得相应金属的为( )
| A. | 加热氧化镁 | B. | 加热碳酸钙 | ||
| C. | 电解饱和氯化钠溶液 | D. | 电解熔融氯化镁 |
7.分类是化学学习和研究中的常用手段,下列分类依据和结论都正确的是( )
| A. | 浓HCl、浓H2SO4、浓HNO3均具有氧化性,都属氧化性酸 | |
| B. | 根据分散系是否有丁达尔效应将分散系分为溶液、胶体和浊液 | |
| C. | NaOH、HNO3、NaNO3在水溶液中均能电离出离子,都属离子化合物 | |
| D. | Na2O2、HCl、BaSO4在熔融状态或溶于水时均能导电,都属电解质 |
8.下列有关叙述正确的是( )
| A. | “煤改气”、“煤改电”等改造工程有利于减少雾霾天气 | |
| B. | PM2.5含有的铅、镉、铬、钒、砷等元素均为对人体有害的金属元素 | |
| C. | 田间焚烧秸秆易造成灰霾,灰霾粒子平均直径在1000~2000nm之间,能发生丁达尔效应 | |
| D. | 汽车尾气净化装置可将尾气中的NO和CO等有害气体转化为N2和CO2,该装置中的催化剂可降低NO和CO反应的活化能,有利于提高该反应的平衡转化率 |
 现有aA、bB、cC、dD、eE五种短周期元素,它们都是生命不可缺少的重要元素.已知它们的原子序数有如下关系:a+b=c,a+c=d,c+d=e;B、D、E都有多种同素异形体,B的化合物种类与A的化合物种类何者最多尚有争议.据此,回答下列有关问题:
现有aA、bB、cC、dD、eE五种短周期元素,它们都是生命不可缺少的重要元素.已知它们的原子序数有如下关系:a+b=c,a+c=d,c+d=e;B、D、E都有多种同素异形体,B的化合物种类与A的化合物种类何者最多尚有争议.据此,回答下列有关问题: .
.