题目内容
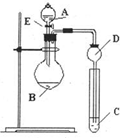 某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用下图装置完成了Cl元素的非金属性比Br强的实验研究.回答下列问题:
某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图装置来一次性完成N、C、Si的非金属性强弱比较的实验研究;乙同学根据置换反应的规律,利用下图装置完成了Cl元素的非金属性比Br强的实验研究.回答下列问题:(1)图中E装置名称是
(2)N、C、Si的非金属性由强到弱的顺序是:
①稀HNO3溶液 ②稀盐酸 ③碳酸钙 ④Na2SiO3溶液 ⑤SiO2
(3)乙同学设计的实验中(酒精灯加热装置在图中未画出),若试剂C为溴化钾溶液溶液外,还需要用到的试剂有:试剂A为
考点:非金属在元素周期表中的位置及其性质递变的规律
专题:实验题
分析:(1)根据装置图结合试验仪器的名称来分析;
(2)根据同周期和同主族元素非金属性的变化规律分析;通过比较酸性强弱来判断非金属性强弱,装置中为强酸制备弱酸依此选择试剂;
(3)通过比较单质的氧化性来判断非金属性:氯气能将溴离子氧化为溴单质可以证明Cl的非金属性比Br强.
(2)根据同周期和同主族元素非金属性的变化规律分析;通过比较酸性强弱来判断非金属性强弱,装置中为强酸制备弱酸依此选择试剂;
(3)通过比较单质的氧化性来判断非金属性:氯气能将溴离子氧化为溴单质可以证明Cl的非金属性比Br强.
解答:
解:(1)由装置图可知,E为加液装置,是分液漏斗;
故答案为:分液漏斗;
(2)同周期从左到右非金属性增强,则C<N,同主族元素从上到下非金属性:C>Si,所以非金属性由强到弱的顺序是:N>C>Si;通过比较酸性强弱来判断非金属性强弱,装置中为强酸制备弱酸,所以A中试剂为稀硝酸,B中为碳酸钙,C中为Na2SiO3溶液;
故答案为:N>C>Si;①;④;
(3)可以用二氧化锰和浓盐酸反应生成氯气,氯气能将溴离子氧化为溴单质来证明Cl的非金属性比Br强,故答案为:浓盐酸;二氧化锰.
故答案为:分液漏斗;
(2)同周期从左到右非金属性增强,则C<N,同主族元素从上到下非金属性:C>Si,所以非金属性由强到弱的顺序是:N>C>Si;通过比较酸性强弱来判断非金属性强弱,装置中为强酸制备弱酸,所以A中试剂为稀硝酸,B中为碳酸钙,C中为Na2SiO3溶液;
故答案为:N>C>Si;①;④;
(3)可以用二氧化锰和浓盐酸反应生成氯气,氯气能将溴离子氧化为溴单质来证明Cl的非金属性比Br强,故答案为:浓盐酸;二氧化锰.
点评:本题考查了元素非金属性强弱的比较,侧重于考查学生的实验探究能力,注意方法的积累,题目难度中等.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
工业上利用硅的氧化物制取硅单质,主要反应为:SiO2+2C
Si+2CO↑.该反应中,还原剂是 (填化学式),被还原的物质是 (填化学式);若反应中消耗了1mol C,则生成 mol Si.
| ||
有下列4种燃料电池的工作原理示意图,其中正极反应的产物为水的是( )
A、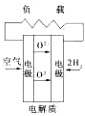 固化氧化物燃料电池 |
B、 碱性氢氧化物电池 |
C、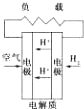 质子交换膜燃料电池 |
D、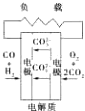 熔融盐燃料电池 |
国家质检部门检出人们端午节包粽子的“返青粽叶”多以硫酸铜为添加剂,长期食用有害健康,请问硫酸铜是一种( )
| A、氧化物 | B、盐 | C、碱 | D、酸 |
银锌电池广泛用作各种电子仪器的电源,它的电池反应是Zn+Ag2OH2O=2Ag+Zn(OH)2则负极上发生反应的物质是( )
| A、Ag |
| B、Zn(OH)2 |
| C、Ag2O |
| D、Zn |
下列关于有机物的说法,正确的是( )
| A、乙醇、乙酸均能与Na反应放出H2,二者分子中官能团相同 |
| B、乙烯和1,3-丁二烯互为同系物,它们均能使Br2水褪色 |
| C、用新制氢氧化铜悬浊液可以鉴别乙酸、乙醛和乙醇三种液体 |
| D、乙酸乙酯中含有的杂质乙酸可用NaOH溶液除去 |