题目内容
下列有关Fe2(SO4)3溶液的叙述正确的是( )
| A、该溶液中,K+、Fe2+、C6H5OH、Br-可以大量共存 |
| B、和KI溶液反应的离子方程式:Fe3++2I-═Fe2++I2 |
| C、和Ba(OH)2溶液反应的离子方程式:Fe3++SO42-+Ba2++3OH-═Fe(OH)3↓+BaSO4↓ |
| D、1L O.1mol?L-1该溶液和足量的Zn充分反应,生成11.2g Fe |
考点:离子共存问题,离子方程式的书写
专题:离子反应专题
分析:A.铁离子能够与苯酚发生显色反应;
B.根据电荷守恒判断,该离子方程式两边电荷不守恒;
C.该离子方程式不满足硫酸铁、氢氧化钡的化学组成关系;
D.根据n=cV计算出硫酸铁及铁离子的物质的量,再根据质量守恒及m=nM计算出铁的质量.
B.根据电荷守恒判断,该离子方程式两边电荷不守恒;
C.该离子方程式不满足硫酸铁、氢氧化钡的化学组成关系;
D.根据n=cV计算出硫酸铁及铁离子的物质的量,再根据质量守恒及m=nM计算出铁的质量.
解答:
解:A.Fe2(SO4)3溶液中的Fe3+与C6H5OH发生显色反应,在溶液中不能大量共存,故A错误;
B.铁离子能够与碘离子发生氧化还原反应,反应的离子方程式为:2Fe3++2I-═2Fe2++I2,题目方程式未配平,故B错误;
C.Fe2(SO4)3溶液和Ba(OH)2溶液反应的生成氢氧化铁沉淀和硫酸钡沉淀,铁离子和硫酸根离子的物质的量的比为2:3,正确的离子方程式为:2Fe3++3SO42-+3Ba2++6OH-═2Fe(OH)3↓+3BaSO4↓,故C错误;
D.1L O.1mol?L-1该溶液中含有溶质硫酸铁0.1mol,0.1mol硫酸铁中含有0.2mol铁离子,与足量锌反应可以生成0.2mol铁,生成铁的质量为11.2g,故D正确;
故选D.
B.铁离子能够与碘离子发生氧化还原反应,反应的离子方程式为:2Fe3++2I-═2Fe2++I2,题目方程式未配平,故B错误;
C.Fe2(SO4)3溶液和Ba(OH)2溶液反应的生成氢氧化铁沉淀和硫酸钡沉淀,铁离子和硫酸根离子的物质的量的比为2:3,正确的离子方程式为:2Fe3++3SO42-+3Ba2++6OH-═2Fe(OH)3↓+3BaSO4↓,故C错误;
D.1L O.1mol?L-1该溶液中含有溶质硫酸铁0.1mol,0.1mol硫酸铁中含有0.2mol铁离子,与足量锌反应可以生成0.2mol铁,生成铁的质量为11.2g,故D正确;
故选D.
点评:本题考查了离子方程式的书写、离子共存的判断,题目难度中等,注意掌握离子反应发生条件,明确常见的离子之间不能共存的情况及离子方程式的书写原则.

练习册系列答案
相关题目
根据下列反应:
①Cu+2FeCl3═2FeCl2+CuCl2
②2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O
③2FeCl2+Cl2═2FeCl3
判断以下各组物质的氧化性由强到弱顺序正确的是( )
①Cu+2FeCl3═2FeCl2+CuCl2
②2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O
③2FeCl2+Cl2═2FeCl3
判断以下各组物质的氧化性由强到弱顺序正确的是( )
| A、KMnO4、FeCl3、Cl2、CuCl2 |
| B、Cl2、FeCl3、KMnO4、CuCl2 |
| C、KMnO4、Cl2、FeCl3、CuCl2 |
| D、CuCl2、FeCl3、Cl2、KMnO4 |
根据卤素性质的递变规律,推测原子半径最大的卤素砹(At)及其化合物不可能具有的性质是( )
| A、砹单质为有色固体,易溶于有机溶剂 |
| B、HAt十分稳定 |
| C、AgAt为有色的、难溶于水的盐 |
| D、NaAt易溶于水 |
下列关于胶体的说法中正确的是( )
| A、胶体区别于其他分散系的本质特征是丁达尔现象 |
| B、利用滤纸可除去淀粉胶体中的少量NaCl |
| C、Fe(OH)3胶体带正电荷 |
| D、将直径为1~100纳米的Fe3O4颗粒均匀分散到水中,将得到Fe3O4胶体 |
下列有关科学家的说法错误的是( )
| A、瑞典化学家舍勒命名了氯元素 |
| B、英国物理学家卢瑟福提出了带核的原子结构模型 |
| C、汤姆生发现电子打破了原子是不可分割的说法 |
| D、德国化学家维勒揭开了人工合成有机物的序幕 |
下列关于氢键的说法中,正确的是( )
| A、氢键比分子间作用力强,所以它属于化学键 |
| B、因为液态水中存在氢键,所以水比硫化氢稳定 |
| C、氨溶于水后氨分子与水分子之间形成氢键 |
| D、邻羟基苯甲醛的熔点比对羟基苯甲醛的熔点高 |
在密闭容器中发生下列反应2A(g)?cC(?)+2D(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述不正确的是( )
| A、C为非气态 |
| B、平衡向逆反应方向移动 |
| C、D的体积分数变小 |
| D、A的转化率变小 |
元素符号、反应方程式、结构示意图、电子式、结构式等通常叫做化学用语.下列有关化学用语的表示方法中错误的是( )
A、异丁烷的结构式: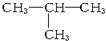 | ||
B、S2-的结构示意图: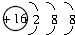 | ||
C、O-18的原子符号:
| ||
| D、CO2分子的结构式:O=C=O |
下列叙述正确的是( )
| A、1.00mol NaCl中含有6.02×1023个NaCl分子 |
| B、1.00mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023 |
| C、欲配置1.00L,1.00mol.L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中 |
| D、用量筒取5.00mL 1.00mol?L-1盐酸于50 mL容量瓶中,加水稀释至刻度,可配制0.100mol?L-1盐酸 |