题目内容
下列电离方程式中,书写正确的是( )
| A、Na2SO4=2Na++SO4-2 |
| B、Ba(OH)2=Ba2++(OH-)2 |
| C、KClO3=K++Cl-+3O2- |
| D、Fe2(SO4)3=2Fe3++3SO42- |
考点:电离方程式的书写
专题:电离平衡与溶液的pH专题
分析:明确电解质的强弱,强电解质完全电离,用等号;弱电解质部分电离,用可逆号,多元弱酸分步电离,原子团不能拆,据此解答.
解答:
解:A.Na2SO4是强电解质完全电离,电离方程式为:Na2SO4=2Na++SO42-,故A错误;
B.Ba(OH)2是强电解质完全电离,电离方程式为:Ba(OH)2=Ba2++2OH-,故B错误;
C.KClO3是强电解质完全电离,电离方程式为:KClO3=K++ClO3-,故C错误;
D.是强电解质完全电离,电离方程式为:Fe2(SO4)3=2Fe3++3SO42-,故D正确;
故选:D.
B.Ba(OH)2是强电解质完全电离,电离方程式为:Ba(OH)2=Ba2++2OH-,故B错误;
C.KClO3是强电解质完全电离,电离方程式为:KClO3=K++ClO3-,故C错误;
D.是强电解质完全电离,电离方程式为:Fe2(SO4)3=2Fe3++3SO42-,故D正确;
故选:D.
点评:本题考查了电离方程式的书写,明确电解质的强弱是解题关键,注意原子团不能拆,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列各组离子可以在溶液中大量共存的是( )
| A、K+、Mg2+、SO42-、OH- |
| B、Na+、H+、Cl-、HCO3- |
| C、K+、Ag+、NO3-、Cl- |
| D、K+、Cu2+、SO42-、NO3- |
有一澄清透明的溶液,只可能含有Fe3+、Fe2+、H+、AlO2-、Al3+、CO32-、NO3-七种离子中的几种,向溶液中逐滴加入一定量1mol/L的NaOH溶液的过程中,开始没有沉淀,而后有沉淀.下列判断正确的是( )
| A、一定不含Fe3+和Fe2+ |
| B、溶液可能含有AlO2- |
| C、溶液可能含有NO3- |
| D、可能含有Fe3+但一定不含Fe2+ |
下列离子或分子在溶液中能大量共存,但通入NO2后会发生化学反应且生成沉淀的一组是( )
| A、Ba2+、Na+、Cl-、HSO3- |
| B、NH4+、K+、ClO-、S2- |
| C、Cu2+、Fe2+、NO3-、SO42- |
| D、Ag+、Na+、NH3?H2O、SO42- |
下列分子式表示的物质一定是纯净物的是( )
| A、CH4 |
| B、C2H6O |
| C、C6H12O6 |
| D、C2H4Cl2 |

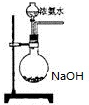 氨在国民经济中占有重要地位.
氨在国民经济中占有重要地位.