题目内容
已知元素周期表中各周期可排元素数目如下:
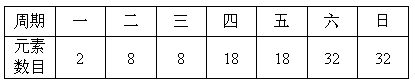
人们预测元素周期表第八周期将来也会排满,那么第八周期排满时元素数目为
[ ]
|
A.32 |
B.42 |
C.46 |
D.50 |
答案:D
解析:
解析:
|
解析:这道题可以从两方面来解决,一是从核外电子的排布规律,二是从一~七周期中元素排列的元素数目.从核外电子的排布规律来看,第七周期排满时的电子层结构为 2、8、18、32、18、8,到第八周期排满时,第八电子层排8种元素,第七电子层作为次外层增加到18,第六电子层作为倒数第三层应增加到32,倒数第四层排满应为50,所以第八周期的元素的数目应为(8+10+14+18)即50种元素.分析一~七周期中元素的数目也可以得出结果,观察每周期元素数目得出,奇数周期的元素数目符合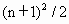 ,偶数周期元素数目符合 ,偶数周期元素数目符合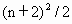 . . |

练习册系列答案
相关题目
(12分)A、B、C、D、E是五种短周期元素。已知:它们的原子序数依次增大,A是元素周期表中原子半径最小的元素;B原子最外层电子数比其次外层电子数多2,C是E的邻族元素;D和E的原子序数之和为30,且D的族序数与周期数相等。甲、乙、丙、丁是它们两两形成的化合物,其中甲分子中含有18个电子。
| 物质组成 | 甲 | 乙 | 丙 | 丁 |
| 化合物中各元素 原子个数比 | A和C 1:1 | B和A 1:4 | D和E 1:3 | B和E 1:4 |
⑴C的氢化物与乙相比较,稳定性强弱关系(用相应的化学式表示): _____>___
⑵元素E在周期表中的位置为第 周期 族
⑶请写出两种与乙具有相同电子数的非单核离子的化学式:_____和_____
⑷把D的单质放到NaOH溶液中,反应的化学方程式为:______________________
⑸写出甲的电子式:________________
⑹有200mL MgCl2和丙的混合溶液,其中c(Mg2+)= 0.2 mol· L-1,c(Cl-)= 1.3 mol·L-1,要使Mg2+全部转化为沉淀分离出来,至少需要4 mol·L-1 NaOH 溶液的体积是: _____
A、B、C、D、E是五种短周期元素。已知:它们的原子序数依次增大,A是元素周期表中原子半径最小的元素;B原子最外层电子数比其次外层电子数多2,C是E的邻族元素;D和E的原子序数之和为30,且D的族序数与周期数相等。甲、乙、 丙、丁是它们两两形成的化合物,其中甲分子中含有18个电子。
| 物质组成 | 甲 | 乙 | 丙 | 丁 |
| 化合物中各元素 原子个数比 | A和C 1:1 | B和A 1:4 | D和E 1:3 | B和E 1:4 |
⑴C的氢化物与乙相比较,稳定性强弱关系(用相应的化学式表示):_____>_ __;
⑵元素E在周期表中的位置为第 周期 族;
⑶请写出两种与乙具有相同电子数的非单核离子的化学式:_____和_____;
⑷把D的单质放到NaOH溶液中,反应的化学方程式为:______________________;
⑸写出甲的电子式:________________;
⑹有200mL MgCl2和丙的混合溶液,其中c(Mg2+)= 0.2 mol· L-1,c(Cl-)= 1.3mol·L-1,要使Mg2+全部转化为沉淀分离出来,至少需要4 mol·L-1 NaOH 溶液的体积是: __ ___。
 E的阴离子结构示意图: (1分)
E的阴离子结构示意图: (1分) 得气体通入1L
得气体通入1L  1mol·L-1
1mol·L-1