题目内容
4.现有浓度均为0.1mol•L-1的四种电解质溶液:①NaHCO3②NaAlO2③CH3COONa ④NaOH
(1)若上述四种溶液pH相同,其物质的量浓度由大到小的顺序是3>1>2>4(填编号).
(2)将四种溶液稀释相同倍数时,其pH变化最大的是4(填编号).
(3)在上述四种溶液中,分别加入FeCl3溶液,能产生的共同现象是生成红褐色沉淀,能产生气体的1(填编号).
分析 (1)电解质溶液:①NaHCO 溶液中碳酸氢根离子水解显碱性,②NaAlO2 溶液中偏铝酸根离子水解显碱性,③CH3COONa 醋酸根离子水解显碱性,④NaOH氢氧化钠是强碱溶液;依据阴离子水解程度分析判断;
(2)四种溶液浓度相同,稀释相同倍数,稀释促进盐类水解,根据是否存在平衡分析判断,不存在平衡的pH值变化大;
(3)碳酸氢根与铁离子发生相互促进水解反应生成氢氧化铁与二氧化碳.
解答 解:(1)氢氧化钠是强碱,不水解,相同浓度的三种溶液氢氧化钠的pH最大,所以pH相同的三种溶液中,氢氧化钠浓度最低,已知酸性:CH3COOH>H2CO3>HAlO2,所以NaAlO2的水解程度大于碳酸氢钠,大于醋酸钠,则当四种溶液的pH相同时,其物质的量浓度由大到小的顺序是3>1>2>4,
故答案为:3>1>2>4;
(2)①NaHCO3②NaAlO2③CH3COONa 都存在水解平衡,当稀释时,盐的弱酸根又水解出部分离子进行补充;氢氧化钠是强碱,完全电离,不存在电离平衡,所以当稀释时,其pH变化最大,
故答案为:4;
(3)碳酸氢根与铁离子发生相互促进水解反应生成氢氧化铁与二氧化碳,NaOH、NaAlO2与CH3COONa和氯化铁反应无气体只生成氢氧化铁沉淀,故答案为:生成红褐色沉淀,1.
点评 本题考查盐类的水解,会运用逆向思维进行分析解答本题,注意盐溶液的碱性强弱取决于阴离子的水解能力,当pH相同时,越难水解的盐,其浓度越大,难度中等.

练习册系列答案
 寒假学与练系列答案
寒假学与练系列答案
相关题目
14.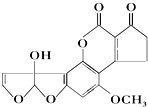 黄曲霉毒素M1是一种具有强致癌性的有机物,其分子结构如图所示.下列有关黄曲霉毒素M1的说法正确的是( )
黄曲霉毒素M1是一种具有强致癌性的有机物,其分子结构如图所示.下列有关黄曲霉毒素M1的说法正确的是( )
 黄曲霉毒素M1是一种具有强致癌性的有机物,其分子结构如图所示.下列有关黄曲霉毒素M1的说法正确的是( )
黄曲霉毒素M1是一种具有强致癌性的有机物,其分子结构如图所示.下列有关黄曲霉毒素M1的说法正确的是( )| A. | 黄曲霉毒素M1的分子式为C17H14O7 | |
| B. | 1mol黄曲霉毒素M1与NaOH溶液发生反应最多能消耗2molNaOH | |
| C. | 黄曲霉毒素M1含有羟基,此羟基能被催化氧化为醛基 | |
| D. | 1mol黄曲霉毒素M1最多能与7molH2发生加成反应 |
15.研究证实,放射性元素${\;}_{53}^{125}$I可以治疗肿瘤,该元素原子的核内中子数是( )
| A. | 72 | B. | 19 | C. | 53 | D. | 125 |
12.下列物质中,主要成分不是硅酸盐的是( )
| A. | 陶瓷 | B. | 大理石 | C. | 玻璃 | D. | 水泥 |
19.C4H9Cl的同分异构体有几种( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
9.下列各组物质中属于同分异构体的是( )
| A. | 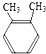 和 和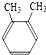 | B. | CH3CH2OH 和 CH3 CH2-O-CH2CH3 | ||
| C. | 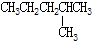 和 和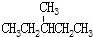 | D. | 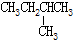 和 和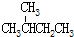 |
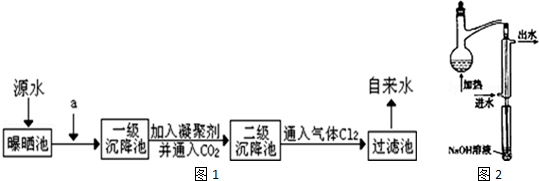
 ,空间构型为平面形.
,空间构型为平面形.