题目内容
14.某电化学装置中发生的总反应式为:Cu+2H+=Cu2++H2↑,下列说法不正确的是( )| A. | a、b不可能是同种材料的电极 | |
| B. | 该装置可能是原电池,也可能是电解池 | |
| C. | 该装置可能是原电池,电解质溶液为稀硝酸 | |
| D. | 该装置的电极可以是铜锌,电解质溶液是稀硫酸 |
分析 电化学装置中发生的总反应式为:Cu+2H+=Cu2++H2↑,Cu与氢离子不能发生自发的氧化还原反应,所以为电解池,则Cu失电子作阳极,阴极上氢离子得电子生成氢气,据此分析.
解答 解:电化学装置中发生的总反应式为:Cu+2H+=Cu2++H2↑,Cu与氢离子不能发生自发的氧化还原反应,所以为电解池,则Cu失电子作阳极,阴极上氢离子得电子生成氢气,
A.阳极为Cu电极,阴极为Cu电极或其它电极材料,所以ab可能是同种材料的电极,故A错误;
B.Cu与氢离子不能发生自发的氧化还原反应,不能构成原电池,所以为电解池,故B错误;
C.Cu与氢离子不能发生自发的氧化还原反应,不能构成原电池,所以为电解池,故C错误;
D.阳极为Cu电极,Cu失电子,Zn为阴极,阴极上氢离子得电子生成氢气,电解质溶液可是稀硫酸,故D正确.
故选D.
点评 本题考查了原电池和电解池原理,根据元素化合价变化确定电极反应,注意能发生自发的氧化还原反应才能构成原电池,题目难度不大.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目
4.近年来我国很多城市发生严重的雾霾天气,对人们的健康造成威胁,下列有关环境问题的说法不正确的是( )
| A. | 改进汽车尾气净化技术,可以减少大气污染物的排放 | |
| B. | PM2.5是指大气中直径小于或等于2.5微米的颗粒物,是雾霾天气产生的主要原因 | |
| C. | 推广燃煤脱硫技术,可以降低SO2对大气的污染 | |
| D. | CO、SO2、NO、NO2都是对大气产生污染的气体,它们在空气中都能稳定存在 |
5.一定温度下,水存在电离平衡H2O(l)?H+(aq)+OH-(aq)△H>0,下列叙述一定正确的是( )
| A. | 向水中加入KHSO4溶液,平衡逆向移动,Kw减小 | |
| B. | 将水加热,Kw增大,pH减小 | |
| C. | 向水中加入少量固体CH3COONa平衡逆向移动,c(H+)降低 | |
| D. | 向水中加入AlCl3溶液,平衡向右移动,KW增大 |
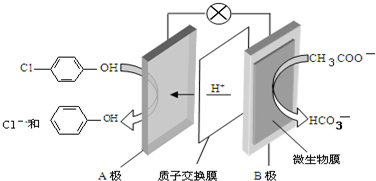
2.现在污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚(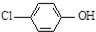 ),其原理如图所示,下列说法正确的是( )
),其原理如图所示,下列说法正确的是( )
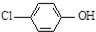 ),其原理如图所示,下列说法正确的是( )
),其原理如图所示,下列说法正确的是( )
| A. | 当外电路中有0.2mole-转移时,A极区增加的H+的个数为0.1NA | |
| B. | A极的电极反应式为 +e-=Cl-+ +e-=Cl-+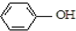 | |
| C. | 电流方向从B极沿导线经小灯泡流向A极 | |
| D. | B为电池的正极,发生还原反应 |
9.下列溶液一定显碱性的是( )
| A. | 含OH-的溶液 | B. | pH>7的溶液 | ||
| C. | c(OH-)>c(H+)的溶液 | D. | 能与金属A1反应放出H2的溶液 |
19.2015年10月,中国中医研究员屠呦呦因发现井提取出青蒿索而获得了诺贝尔医学奖.她发现的青蒿素用以治疗疟疾,挽救了数百万患者的生命.青蒿素的分子式为C5H22O5,它属于( )
| A. | 单质 | B. | 混合物 | C. | 无机物 | D. | 有机物 |
6.常用的中性笔由笔杆、笔套和笔芯构成.笔杆和笔套由塑料注塑成型;笔芯由笔头、笔管和油墨组成,笔头采用铜合金和不锈钢制成;球珠多采用不锈钢、硬质合金或氧化铝等材料制成;笔芯内是一种有机溶剂,所以被称为中性笔.下列不属于有机高分子合成材料的是( )
| A. | 笔杆 | B. | 笔套 | C. | 笔头 | D. | 笔管 |
4.下列实验装置能达到实验目的是( )
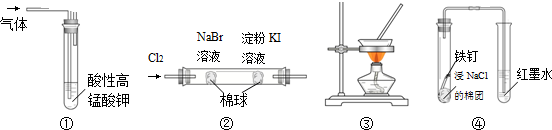

| A. | 图①装置可用于除去甲烷中混有的乙烯 | |
| B. | 图②装置可证明氧化性:Cl2>Br2>I2 | |
| C. | 图③装置可通过蒸干AlCl3饱和溶液制备AlCl3晶体 | |
| D. | 图④装置可观察铁的吸氧腐蚀 |