题目内容
18.溴“海洋元素”之称.实验室模拟海水中溴的提取,实验方法:将适量新制氯水加人20mL富含溴离子的海水中(海水可以用0.1mol•L-1、的NaBr溶液代替),把溴置换出来,氯水中的氯气作氧化剂,涉及反应的离子方程式为Cl2+2Br-=Br2+2Cl-.得到的单质溴可以用有机溶剂在分液漏斗(仪器)中实现萃取富集,萃取试剂用CCl4、苯等,得到的有机层显橙红色.分析 氯水中的氯气氧化性大于溴单质,可以优惠溴离子生成溴单质,利用单质溴在水中和其他溶剂中溶解度的不同提纯溴,为萃取,常用仪器为分液漏斗,萃取剂一般为四氯化碳、苯等有机溶剂,溴单质被四氯化碳萃取溶液显橙红色;
解答 解:将适量新制氯水加人20mL富含溴离子的海水中(海水可以用0.1mol•L-1、的NaBr溶液代替),把溴置换出来,反应的离子方程式为:Cl2+2Br-=Br2+2Cl-,反应中氯元素化合价0价变化为-1价做氧化剂,得到溴单质可以用有机溶剂四氯化碳或苯在分液漏斗中萃取分液分离,溴单质被四氯化碳萃取溶液显橙红色,
故答案为:氧化;Cl2+2Br-=Br2+2Cl-;分液漏斗;CCl4;橙红色;
点评 本题考查了海水提溴的原理和提取实验基本操作,主要是仪器和试剂的选择,掌握基础是解题关键,题目较简单.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
8.某兴趣小组在利用图1所示装置做铜与稀硝酸反应的实验中,发现开始时气泡产生速率非常慢,一段时间后速率明显加快,烧瓶内溶液呈浅蓝色并不断加深,液面上方的气体颜色也在不断加深.该小组同学拟通过实验探究反应速率变化的原因.

(1)图1中铜与稀硝酸反应的离子方程式为3Cu+8H++2NO3-(稀)═3Cu2++2NO↑+4H2O.
(2)图1中NaOH溶液能够吸收的有害气体是二氧化氮和一氧化氮气体.
(3)小组同学提出了如下假设并设计实验探究:
Ⅰ.甲同学认为反应速率变化的原因可能是反应放热导致溶液温度升高所致,故测定反应过程中溶液不同时间的温度,结果如下表:
结合实验目的和表中数据,你得出的结论是温度不是反应速率明显加快的主要原因.
Ⅱ.乙同学认为生成的Cu2+对反应有催化作用,为验证此假设,取A、B两支试管分别加入等量的铜片和稀硝酸,那么最好是在其中一支试管中加入少量的A(填序号).
A.硝酸铜晶体 B.硝酸铜溶液 C.硫酸铜晶体 D.硫酸铜溶液
然后对比两支试管的反应,发现现象基本相同.故得出结论:Cu2+并不是反应的催化剂.
Ⅲ.丙同学根据现象推测反应过程中还有少量NO2生成,进而认为该物质对反应有催化作用,如图2所示,丙同学从a处通入该物质后,发现左管中产生气泡速率明显快于右管.小组同学得出最后结论:这种物质对铜和稀硝酸的反应有催化作用.
(4)实验结束后,发现试管中溶液呈绿色,而不显蓝色.部分同学认为是该溶液中Cu2+的浓度较高所致,另一部分同学认为是该溶液中溶解了通入的物质.丁同学设计了一个实验方案证明后者的推测更为合理.(在表格中写出该同学可能的实验操作和实验现象)

(1)图1中铜与稀硝酸反应的离子方程式为3Cu+8H++2NO3-(稀)═3Cu2++2NO↑+4H2O.
(2)图1中NaOH溶液能够吸收的有害气体是二氧化氮和一氧化氮气体.
(3)小组同学提出了如下假设并设计实验探究:
Ⅰ.甲同学认为反应速率变化的原因可能是反应放热导致溶液温度升高所致,故测定反应过程中溶液不同时间的温度,结果如下表:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 35 | 50 | 60 | 70 | 80 |
| 温度/℃ | 25 | 26 | 26 | 26 | 26 | 26 | 26.5 | 27 | 27 | 27 | 27 |
Ⅱ.乙同学认为生成的Cu2+对反应有催化作用,为验证此假设,取A、B两支试管分别加入等量的铜片和稀硝酸,那么最好是在其中一支试管中加入少量的A(填序号).
A.硝酸铜晶体 B.硝酸铜溶液 C.硫酸铜晶体 D.硫酸铜溶液
然后对比两支试管的反应,发现现象基本相同.故得出结论:Cu2+并不是反应的催化剂.
Ⅲ.丙同学根据现象推测反应过程中还有少量NO2生成,进而认为该物质对反应有催化作用,如图2所示,丙同学从a处通入该物质后,发现左管中产生气泡速率明显快于右管.小组同学得出最后结论:这种物质对铜和稀硝酸的反应有催化作用.
(4)实验结束后,发现试管中溶液呈绿色,而不显蓝色.部分同学认为是该溶液中Cu2+的浓度较高所致,另一部分同学认为是该溶液中溶解了通入的物质.丁同学设计了一个实验方案证明后者的推测更为合理.(在表格中写出该同学可能的实验操作和实验现象)
| 操作 | 现象 |
| 向该绿色溶液中通入氮气(或向硝酸铜溶液中通入浓硝酸与铜反应产生的气体) | 溶液颜色变蓝(或绿色加深) |
9.下列说法正确的是( )
| A. | 石油液化气、汽油和石蜡的主要成分都是碳氢化合物 | |
| B. | CH3-CH=CH-CH3与C3H6一定互为同系物 | |
| C. | 用浸泡过高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的 | |
| D. | 等质量的乙烯和聚乙烯充分燃烧所需氧气的量不相等 |
6.已知H2O2的分子结构可表示为H-O-O-H,设H2O2中H、O两元素是由${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、${\;}_{8}^{16}$O、${\;}_{8}^{18}$O四种核素组成,则共有H2O2分子的种类是( )
| A. | 8种 | B. | 9种 | C. | 10种 | D. | 11种 |
3.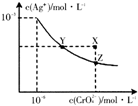 已知t℃时,AgCl的Ksp=2×10-10,Ag2CrO4(橙红色固体)在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )
已知t℃时,AgCl的Ksp=2×10-10,Ag2CrO4(橙红色固体)在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )
 已知t℃时,AgCl的Ksp=2×10-10,Ag2CrO4(橙红色固体)在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )
已知t℃时,AgCl的Ksp=2×10-10,Ag2CrO4(橙红色固体)在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是( )| A. | t℃时,AgCl在水中的溶解度比在稀盐酸中小 | |
| B. | t℃时,AgCl的溶解度大于Ag2CrO4 | |
| C. | 在饱和Ag2CrO4溶液中加入少量K2CrO4,可使溶液由Y点移至X点 | |
| D. | 向同浓度NaCl和K2CrO4混合液中,滴加0.1mol•L-1AgNO3溶液,先生成白色沉淀 |
10.根据侯氏制碱原理制备少量NaHCO3的实验,经过制取氨气、制取NaHCO3、分离NaHCO3、干燥NaHCO3四个步骤,下列图示装置和原理能达到实验目的是( )
| A. | 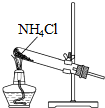 制取氨气 | B. | 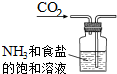 制取NaHCO3 | C. | 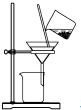 分离NaHCO3 | D. |  干燥NaHCO3 |
7.下列情况会导致食品对人体有害的是( )
①将鸡蛋浸泡在石灰水中防止变质②罐装食品中加化学防腐剂③用稀KMnO4溶液洗涤蔬菜④食盐中加KIO3制成碘盐⑤用SO2漂白粉条⑥用福尔马林浸泡海产品.
①将鸡蛋浸泡在石灰水中防止变质②罐装食品中加化学防腐剂③用稀KMnO4溶液洗涤蔬菜④食盐中加KIO3制成碘盐⑤用SO2漂白粉条⑥用福尔马林浸泡海产品.
| A. | ①②③⑤⑥ | B. | ②③④⑤⑥ | C. | ②⑤⑥ | D. | ①②⑤⑥ |
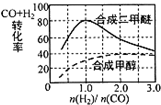 碳和碳的化合物在生产、生活中有重要作用,甲醇水蒸气重整制氢系统可能发生下列三个反应:
碳和碳的化合物在生产、生活中有重要作用,甲醇水蒸气重整制氢系统可能发生下列三个反应: