题目内容
6.将氢氧化钠溶液滴入某浓度的盐酸、氯化镁和氯化铝的混合溶液中,直至过量,则下列图象变化趋势正确的是( )| A. | 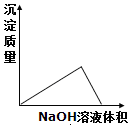 | B. | 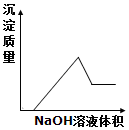 | C. | 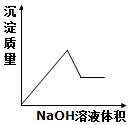 | D. |  |
分析 将氢氧化钠溶液滴入某浓度的盐酸、氯化镁和氯化铝的混合溶液中,盐酸先与氢氧化钠溶液反应生成氯化钠和水,然后氯化镁和氢氧化钠生成氯化钠和氢氧化镁沉淀,氯化铝和氢氧化钠生成氯化钠和氢氧化铝沉淀;当沉淀达到最大后,由于氢氧化铝和过量的氢氧化钠生成偏铝酸钠和水,会有部分沉淀溶解,据此进行解答.
解答 解:将氢氧化钠溶液滴入某混有盐酸的氯化镁和氯化铝的混合溶液中,盐酸优先与NaOH溶液反应,所以开始时不会生成沉淀;
当盐酸完全反应后,镁离子、铝离子与氢氧化钠反应生成氢氧化镁、氢氧化铝沉淀;
当镁离子、铝离子完全反应后,氢氧化铝与过量的氢氧化钠溶液反应,导致沉淀部分水解,图象中沉淀的量减少,
根据分析可知,满足以上变化的图象为B,
故选B.
点评 本题考查了镁、铝重要化合物的性质,题目难度不大,明确发生反应的先后顺序为解答关键,注意掌握氢氧化铝具有两性,试题有利于提高学生的分析能力及灵活应用基础知识的能力.

练习册系列答案
相关题目
16.卤素互化物(XX′n)的性质与卤素单质相似,其中非金属性:X<X′.已知反应如下:3H2O+2ICl3=5HCl+ICl+HIO3.则下列判断正确的是( )
| A. | XX′n 属于活泼非金属单质 | |
| B. | ICl3 属于共价化合物 | |
| C. | 上述反应中HCl是还原产物 | |
| D. | ICl溶于水的反应:ICl+H2O=HIO+HCl 不属于氧化还原反应 |
17.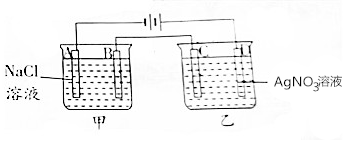 按如图进行电解实验(A,B,C,D均为惰性电极).
按如图进行电解实验(A,B,C,D均为惰性电极).
电极反应式:
A极:2H++2e-═H2↑;
B极:2Cl--2e-=Cl2↑;
C极:Ag++e-═Ag;
D极:4OH--4e-═2H2O+O2↑.
 按如图进行电解实验(A,B,C,D均为惰性电极).
按如图进行电解实验(A,B,C,D均为惰性电极).电极反应式:
A极:2H++2e-═H2↑;
B极:2Cl--2e-=Cl2↑;
C极:Ag++e-═Ag;
D极:4OH--4e-═2H2O+O2↑.
14.下列说法正确的是( )
| A. | 某溶液加入足量硝酸银溶液产生白色沉淀,证明其中一定存在Cl- | |
| B. | 某溶液加入足量稀盐酸无现象,再加入BaCl2产生白色沉淀,证明其中一定存在SO42- | |
| C. | 某溶液加人稀盐酸产生无色、无味能使澄请石灰水变混浊的气体,证明其中一定存在CO32- | |
| D. | 向品红溶液中通入某气体后,品红溶液红色消失,证明该气体一定是SO2 |
1.在实验室中,对下列事故或药品的处理正确的是( )
| A. | 金属钠失火时立即用水灭火,然后用稀硫酸中和 | |
| B. | 为了防止挥发,氢氧化钠溶液保存在用磨砂玻璃塞的玻璃试剂瓶中 | |
| C. | 少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 | |
| D. | 配置一定物质的量浓度溶液时,不慎将少量水加过刻度线,应重新配置 |
11.下列各溶液中,Na+物质的量浓度最大的是( )
| A. | 200 mL 0.5mol/LNaCl溶液 | B. | 50 mL 0.3mol/LNa2SO4溶液 | ||
| C. | 150 mL 0.4mol/LNaOH | D. | 200mL0.15mol/LNa3PO4 |
18.如图所示装置中发生反应的离子方程式为:Zn+2H+=Zn2++H2↑,下列说法错误的是( )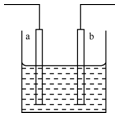

| A. | a,b可能是同种材料的电极 | |
| B. | 该装置可能是电解池,电解质溶液为稀硝酸 | |
| C. | 该装置可能是原电池,电解质溶液为稀盐酸 | |
| D. | 该装置可看作是铜一锌原电池,电解质溶液是稀硫酸 |
2.下列分子或离子在指定的分散系中能大量共存的一组是( )
| A. | 偏铝酸钠溶液:K+、NO3-、NH3•H2O | |
| B. | 空气:C2H6、CO2、SO2、NO | |
| C. | 硫酸铜溶液:H+、K+、S2-、Br- | |
| D. | 重铬酸钾钾溶液:H+、Na+、SO42-、乙醛分子 |