题目内容
下列反应中,属于非氧化还原反应的是( )
| A、3Cl2+6NaOH=5NaCl+NaClO3+3H2O |
| B、2Br-+Cl2=2Cl-+Br2 |
| C、CaCO3+2HCl=CaCl2+H2O+CO2 |
| D、CO2+Na2O2=Na2CO3+O2 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:属于氧化还原反应,说明该反应中有元素化合价升降,非氧化还原反应,则反应中没有元素化合价的变化,据此分析解答.
解答:
解:A.3Cl2+6NaOH=5NaCl+NaClO3+3H2O中各Cl元素的化合价发生变化,所以属于氧化还原反应,故A不选;
B.2Br-+Cl2=2Cl-+Br2中Br、Cl元素化合价变化,则属于氧化还原反应,故B不选;
C.CaCO3+2HCl=CaCl2+H2O+CO2 中各元素化合价不变,属于非氧化还原反应,故C选;
D.2CO2+2Na2O2=2Na2CO3+O2中O元素化合价发生变化,所以属于氧化还原反应,故D不选;
故选C.
B.2Br-+Cl2=2Cl-+Br2中Br、Cl元素化合价变化,则属于氧化还原反应,故B不选;
C.CaCO3+2HCl=CaCl2+H2O+CO2 中各元素化合价不变,属于非氧化还原反应,故C选;
D.2CO2+2Na2O2=2Na2CO3+O2中O元素化合价发生变化,所以属于氧化还原反应,故D不选;
故选C.
点评:本题考查了氧化还原反应判断,根据元素化合价变化来分析解答即可,知道常见元素化合价及常见反应类型,题目难度不大.

练习册系列答案
相关题目
下列叙述正确的是( )
A、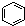 和 和 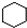 均是芳香烃, 均是芳香烃,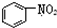 既是芳香烃又是芳香化合物 既是芳香烃又是芳香化合物 |
| B、分子式为C3H6Cl2的有机物共有5种同分异构体(不考虑立体异构) |
| C、分子式为C4H8有机物最多存在4个C-C单键 |
| D、分子式为C2H6O的红外光谱图上发现有C-H键和C-O键的振动吸收,由此可推测有机物结构简式为C2H5-OH |
下列操作中,能使电离平衡H2O?H++OH-向右移动且溶液呈酸性的是( )
| A、向水中加入NaHSO4溶液 |
| B、将水加热到100℃,使pH=6 |
| C、向水中加入Al2(SO4)3固体 |
| D、向水中加入CH3COONa固体 |
下列分子式表示的物质一定是纯净物的是( )
| A、C5H10 |
| B、C7H8O |
| C、CH4O |
| D、C2H4O2 |
在甲、乙、丙、丁四个烧杯里分别放入0.1mol的钠,氧化钠,过氧化钠和氢氧化钠,然后各加入100mL水,使固体完全溶解,则甲、乙、丙、丁的溶液中溶质的质量分数大小的顺序为( )
| A、甲>乙>丙>丁 |
| B、丁<甲<乙=丙 |
| C、甲=丁<乙=丙 |
| D、丁<甲<乙<丙 |
下列物质中,既能跟盐酸反应,又能跟氢氧化钠溶液反应的是( )
| A、Na2CO3 |
| B、NaHCO3 |
| C、Fe2O3 |
| D、CO2 |
mg铁粉与含有H2SO4的CuSO4溶液完全反应后,得到mg铜,则参与反应的CuSO4与H2SO4的物质的量之比为( )
| A、7:1 | B、1:7 |
| C、7:8 | D、8:7 |
