题目内容
下列叙述中,错误的是( )
| A、阿伏加德罗常数的符号为NA,其近似值为6.02×1023 mol-1 |
| B、等物质的量的O2与O3,所含氧原子数相同 |
| C、在0.5 mol Na2SO4中,含有的Na+数约是6.02×1023 |
| D、摩尔是物质的量的单位 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.根据阿伏伽德罗常数的符号及近似值进行判断;
B.氧气和臭氧分子中含有的氧原子数目不同,等物质的量的二者中含有的氧原子数目一定不同;
C.0.5mol硫酸钠中含有1mol钠离子;
D.物质的量为基本物理量,物质的量的单位为mol.
B.氧气和臭氧分子中含有的氧原子数目不同,等物质的量的二者中含有的氧原子数目一定不同;
C.0.5mol硫酸钠中含有1mol钠离子;
D.物质的量为基本物理量,物质的量的单位为mol.
解答:
解:A.阿伏加德罗常数的符号为NA,6.02×1023mol-1为阿伏伽德罗常数的近似值,故A正确;
B.1mol氧气中含有2mol氧原子,1mol臭氧中含有3mol氧原子,所以等物质的量的O2与O3,所含氧原子数不同,故B错误;
C.0.5 mol Na2SO4中含有1mol钠离子,含有的Na+数约是6.02×1023,故C正确;
D.物质的量为国际单位制中七个基本物理量之一,其单位为摩尔,故D正确;
故选B.
B.1mol氧气中含有2mol氧原子,1mol臭氧中含有3mol氧原子,所以等物质的量的O2与O3,所含氧原子数不同,故B错误;
C.0.5 mol Na2SO4中含有1mol钠离子,含有的Na+数约是6.02×1023,故C正确;
D.物质的量为国际单位制中七个基本物理量之一,其单位为摩尔,故D正确;
故选B.
点评:本题考查阿伏加德罗常数、物质的量与摩尔的关系,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确物质的量与摩尔之间的正确关系.

练习册系列答案
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
设NA为阿伏加德罗常数的值,下列叙述中正确的是( )
| A、1.2 g镁在足量的氮气中燃烧,镁失去的电子数为0.2NA |
| B、0.1 mol/L氢氧化钠溶液中所含Na+数为0.1NA |
| C、11.2 L二氧化碳中所含有的氧原子数为NA |
| D、46g NO2和N2O4的混合气体中含有的原子个数为3NA |
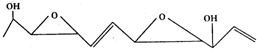
有一种有机物结构简式为 推测下列说法不正确的是( )
推测下列说法不正确的是( )
 推测下列说法不正确的是( )
推测下列说法不正确的是( )| A、易溶于水,也易溶于有机溶剂 |
| B、能使溴水和酸性高锰酸钾溶液褪色 |
| C、能发生加聚反应 |
| D、在分子中,位于同一平面上的原子数最多可能是19个 |
在理论上不能用于设计原电池的化学反应是( )
| A、HCl ( aq )+NaOH ( aq )=NaCl ( aq )+H2O ( l )△H<0 |
| B、2CH3OH ( l )+3O2 ( g )=2CO2 ( g )+4H2O ( l )△H<0 |
| C、4Fe (OH)2( s )+2H2O ( l )+O2( g )=4Fe (OH)3( s )△H<0 |
| D、2H2( g )+O2( g )=2H2O ( l )△H<0 |
下列有关气体体积的叙述中,正确的是( )
| A、一定温度和压强下,各种气态物质的体积大小由构成气体的分子大小决定 |
| B、一定温度和压强下,各种气态物质的体积大小由构成气体的分子数决定 |
| C、非标准状况下,1 mol任何气体的体积不可能为22.4 L |
| D、0.5 mol气体A和0.5 mol气体B的混合气体在标准状况下的体积不一定为22.4 L |
常温下,某溶液中由水电离产生的c(OH-)=10-10 mol/L,则此溶液可能是( )
| A、NaOH |
| B、CH3COONa |
| C、HCl |
| D、NH4Cl |
下列物质属于芳香醇的是( )
| A、CH3-C6H4-CH2-OH |
| B、CH3-C6H4-OCH3 |
| C、CH3-(CH2)6-OH |
| D、CH3-C6H4-OH |
下列是一些常用的危险品图标,装运浓硫酸的箱子应贴的图标是( )
A、 |
B、 |
C、 |
D、 |
 已知:
已知: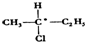 就有光学活性.标有“*”号的碳原子叫手性碳原子.
就有光学活性.标有“*”号的碳原子叫手性碳原子.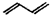 .
.