题目内容
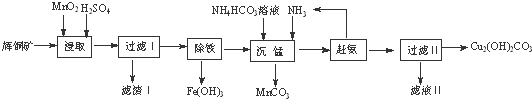
蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成.由蛇纹石制取碱式碳酸镁的实验步骤如下:
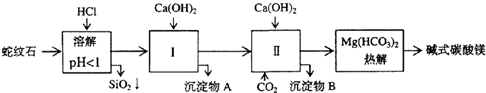
(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是 .
(2)从沉淀混合物A[含有Fe(OH)3和Al(OH)3]中提取红色氧化物作颜料,先向沉淀物A中加入 溶液 (填入物质的化学式),然后 、 、 (依次填写实验操作名称).
(3)物质循环使用,能节约资源.上述实验中,可以循环使用的物质是 (填写物质化学式).
(4)18.2g产品碱式碳酸镁:aMgCO3?bMg(OH)2?cH2O完全分解后,产生6.6g CO2和8.0g MgO,由此可知,产品的化学式中:a= 、b= 、c= .

(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是
(2)从沉淀混合物A[含有Fe(OH)3和Al(OH)3]中提取红色氧化物作颜料,先向沉淀物A中加入
(3)物质循环使用,能节约资源.上述实验中,可以循环使用的物质是
(4)18.2g产品碱式碳酸镁:aMgCO3?bMg(OH)2?cH2O完全分解后,产生6.6g CO2和8.0g MgO,由此可知,产品的化学式中:a=
考点:物质分离和提纯的方法和基本操作综合应用,制备实验方案的设计
专题:实验设计题
分析:蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成,酸溶过滤得到滤液中为Mg2+、Fe3+、Al3+,加入氢氧化钙沉淀得到氢氧化铝、氢氧化铁沉淀A,滤液中通入二氧化碳生成氢氧化铝沉淀B和碳酸氢钙,加入氢氧化钙反应生成碳酸钙循环利用,溶液中得到碳酸氢镁溶液,热解得到碱式碳酸镁;
(1)蛇纹石矿可以看做MgO、Fe2O3、Al2O3、SiO2组成,蛇纹石加盐酸溶解后,MgO、Fe2O3、Al2O3和HCl反应溶解,而SiO2和HCl不反应,不能溶解;
(2)红色氧化物为Fe2O3,应先将其中含有的少量Al(OH)3除去,除去Al(OH)3的方法是利用它能溶于强碱的性质;
(3)此过程中CO2是可以重复使用的;
(4)确定产品aMgCO3?bMg(OH)2?cH2O中a、b、c的值,需要测定的数据是①样品质量;②MgO质量;③生成CO2的质量(或体积);④生成水的质量;
(1)蛇纹石矿可以看做MgO、Fe2O3、Al2O3、SiO2组成,蛇纹石加盐酸溶解后,MgO、Fe2O3、Al2O3和HCl反应溶解,而SiO2和HCl不反应,不能溶解;
(2)红色氧化物为Fe2O3,应先将其中含有的少量Al(OH)3除去,除去Al(OH)3的方法是利用它能溶于强碱的性质;
(3)此过程中CO2是可以重复使用的;
(4)确定产品aMgCO3?bMg(OH)2?cH2O中a、b、c的值,需要测定的数据是①样品质量;②MgO质量;③生成CO2的质量(或体积);④生成水的质量;
解答:
解:(1)蛇纹石加盐酸溶解,MgO、Fe2O3、Al2O3和HCl反应溶解,反应方程式分别为:MgO+2HCl=MgCl2+H2O,Fe2O3+6HCl=2FeCl3+3H2O,Al2O3+6HCl=2AlCl3+3H2O.而SiO2不与盐酸反应,以沉淀的形式除去,故答案为:Fe3+、Al3+;
(2)从实验步骤图知:沉淀混合物为Fe(OH)3和Al(OH)3,红色氧化物是沉淀物Fe(OH)3分解后得到的Fe2O3,所以得先加碱把Al(OH)3除掉,反应为:Al(OH)3+NaOH=NaAlO2+2H2O,然后过滤洗涤灼烧即可;
故答案为:NaOH;过滤、洗涤、灼烧;
(3)从实验步骤图知:上述实验中,步骤Ⅱ中通二氧化碳,生成碳酸钙,碳酸钙分解可得到二氧化碳,作为第Ⅱ步的原料,碱式碳酸镁分解得到CO2,可以循环使用的物质是CaCO3或CO2;
故答案为:CaCO3或CO2;
(4)m(样品)=18.2g,m(CO2)=6.6g,m(MgO)=8.0g,碱式碳酸镁分解:aMgCO3?bMg(OH)2?cH2O
(a+b)MgO+aCO2↑+(b+c)H2O↑,根据质量守恒得:m(H2O)=18.2g-6.6g-8.0g=3.6g,则m(MgO)═0.2mol,n(CO2)═0.15mol,n(H2O)═0.2mol,得:a:b:c=0.15:0.05:0.15=3:1:3,故答案为:3,1,3;
(2)从实验步骤图知:沉淀混合物为Fe(OH)3和Al(OH)3,红色氧化物是沉淀物Fe(OH)3分解后得到的Fe2O3,所以得先加碱把Al(OH)3除掉,反应为:Al(OH)3+NaOH=NaAlO2+2H2O,然后过滤洗涤灼烧即可;
故答案为:NaOH;过滤、洗涤、灼烧;
(3)从实验步骤图知:上述实验中,步骤Ⅱ中通二氧化碳,生成碳酸钙,碳酸钙分解可得到二氧化碳,作为第Ⅱ步的原料,碱式碳酸镁分解得到CO2,可以循环使用的物质是CaCO3或CO2;
故答案为:CaCO3或CO2;
(4)m(样品)=18.2g,m(CO2)=6.6g,m(MgO)=8.0g,碱式碳酸镁分解:aMgCO3?bMg(OH)2?cH2O
| ||
点评:本题主要考查了元素化合物中金属铝、铁的性质,解题时不仅需熟知物质间的反应原理,还需灵活运用于实验的设计,题目难度中等.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、氯气、SO2都具有氧化性,故而可用于漂白纸浆等 |
| B、常温下浓硫酸能与铝发生钝化,可在常温下用铝制容器贮运浓硫酸 |
| C、H2CO3是弱酸,所以NaHCO3是弱电解质 |
| D、较强的酸可以制取较弱的酸,次氯酸溶液无法制取盐酸 |
下列属于电解质并能导电的物是( )
①熔融的NaCl ②KNO3溶液 ③Cu ④酒精 ⑤NaCl晶体 ⑥盐酸.
①熔融的NaCl ②KNO3溶液 ③Cu ④酒精 ⑤NaCl晶体 ⑥盐酸.
| A、① | B、①②③⑤⑥ |
| C、①②⑥ | D、①③④⑤ |
实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是( )
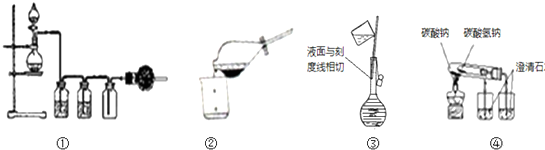

| A、①可用于实验室用MnO2固体与浓盐酸反应,制取并收集干燥、纯净的Cl2 |
| B、②从溴水中萃取溴后的分离操作 |
| C、③配制1mol/LNaCl溶液定容操作 |
| D、用图④操作可比较Na2CO3与NaHCO3的热稳定性 |
通以相等的电量,分别电解等浓度的硝酸银和硝酸亚汞(亚汞的化合价为+1)溶液,若被还原的硝酸银和硝酸亚汞的物质的量之比n(硝酸银):n(硝酸亚汞)=2:1,则下列叙述正确的是( )
| A、电解后溶液的pH都增大 |
| B、在两个阳极上得到的产物的物质的量不相等 |
| C、硝酸亚汞的分子式为Hg2(NO3)2 |
| D、在两个阴极上得到的银和汞的物质的量之比为2:1 |
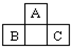 如图为短周期一部分.A、C两元素原子核外分别有两个、一个未成对电子.试回答:
如图为短周期一部分.A、C两元素原子核外分别有两个、一个未成对电子.试回答: