��Ŀ����
���ж�����������������ȷ�Ĵ̡�������Ĵ�������
��1��1mol����1mol����ȫ��Ӧ�ų����������к��ȣ�
��2�����ʾ��е�����Խ�ߣ����ʵ��ȶ���Խǿ��
��3����ѧ��Ӧ�Ĺ��̣�����ѭ�����غ㶨�ɣ�Ҳ��ѭ�����غ㶨�ɣ�
��4����ȷ���Ļ�ѧ��Ӧ��ϵ�У���Ӧ������������������������һ����ͬ��
��5����Ҫ���Ȳ��ܽ��еķ�Ӧһ�������ȷ�Ӧ��
����֪���з�Ӧ�ķ�Ӧ��Ϊ��
��1��CH3COOH��l��+2O2��g���T2CO2��g��+2H2O��l����H1=-870.3kJ?mol-1
��2��C��s��+O2��g���TCO2��g����H=-393.5kJ?mol-1
��3��H2��g��+
O2��g���TH2O��l����H=-285.8kJ?mol-1
�Լ������з�Ӧ�ķ�Ӧ�ȣ�2C��s��+2H2��g��+O2��g���TCH3COOH��l����H= ��
��1��1mol����1mol����ȫ��Ӧ�ų����������к��ȣ�
��2�����ʾ��е�����Խ�ߣ����ʵ��ȶ���Խǿ��
��3����ѧ��Ӧ�Ĺ��̣�����ѭ�����غ㶨�ɣ�Ҳ��ѭ�����غ㶨�ɣ�
��4����ȷ���Ļ�ѧ��Ӧ��ϵ�У���Ӧ������������������������һ����ͬ��
��5����Ҫ���Ȳ��ܽ��еķ�Ӧһ�������ȷ�Ӧ��
����֪���з�Ӧ�ķ�Ӧ��Ϊ��
��1��CH3COOH��l��+2O2��g���T2CO2��g��+2H2O��l����H1=-870.3kJ?mol-1
��2��C��s��+O2��g���TCO2��g����H=-393.5kJ?mol-1
��3��H2��g��+
| 1 |
| 2 |
�Լ������з�Ӧ�ķ�Ӧ�ȣ�2C��s��+2H2��g��+O2��g���TCH3COOH��l����H=
���㣺��Ӧ�Ⱥ��ʱ�,�Ȼ�ѧ����ʽ
ר�⣺��ѧ��Ӧ�е������仯
�������٣�1�����к��ȵĸ��������
��2�����ʵ�����Խ��Խ�ȶ���
��3����ѧ��Ӧ��ѭ�����غ㶨�ɺ������غ㶨�ɣ�
��4���κλ�ѧ��Ӧ���������仯��
��5����Ӧ���뷴Ӧ�����أ�
��������֪��Ӧ���ݸ�˹���ɽ��
��2�����ʵ�����Խ��Խ�ȶ���
��3����ѧ��Ӧ��ѭ�����غ㶨�ɺ������غ㶨�ɣ�
��4���κλ�ѧ��Ӧ���������仯��
��5����Ӧ���뷴Ӧ�����أ�
��������֪��Ӧ���ݸ�˹���ɽ��
���
�⣺�٣�1���к�����ָǿ��ǿ���ϡ��Һ�к�����1molˮʱ�ų����������ʣ�1������
��2�����ʵ�����Խ��Խ�ȶ����ʣ�2������
��3���κλ�ѧ��Ӧ����ѭ�����غ㶨�ɺ������غ㶨�ɣ��ʣ�3���̣�
��4���κλ�ѧ��Ӧ�ж��������仯�����Է�Ӧ��������������һ����ͬ���ʣ�4���̣�
��5��ȼ�ն��Ƿ��ȷ�Ӧ������ȵ��Ż�㣬�ʣ�5������
����֪��1��CH3COOH��l��+2O2��g���T2CO2��g��+2H2O��l����H1=-870.3kJ?mol-1
��2��C��s��+O2��g���TCO2��g����H=-393.5kJ?mol-1
��3��H2��g��+
O2��g���TH2O��l����H=-285.8kJ?mol-1
�ݸ�˹���ɣ���2����2+��3����2-��1���ã�
2C��s��+2H2��g��+O2��g���TCH3COOH��l����H=-488KJ/mol��
�ʴ�Ϊ��-488.3 kJ?mol-1��
��2�����ʵ�����Խ��Խ�ȶ����ʣ�2������
��3���κλ�ѧ��Ӧ����ѭ�����غ㶨�ɺ������غ㶨�ɣ��ʣ�3���̣�
��4���κλ�ѧ��Ӧ�ж��������仯�����Է�Ӧ��������������һ����ͬ���ʣ�4���̣�
��5��ȼ�ն��Ƿ��ȷ�Ӧ������ȵ��Ż�㣬�ʣ�5������
����֪��1��CH3COOH��l��+2O2��g���T2CO2��g��+2H2O��l����H1=-870.3kJ?mol-1
��2��C��s��+O2��g���TCO2��g����H=-393.5kJ?mol-1
��3��H2��g��+
| 1 |
| 2 |
�ݸ�˹���ɣ���2����2+��3����2-��1���ã�
2C��s��+2H2��g��+O2��g���TCH3COOH��l����H=-488KJ/mol��
�ʴ�Ϊ��-488.3 kJ?mol-1��
���������⿼�����к��ȡ����ʵ�����Խ��Խ�ȶ�����Ӧ�ȡ���˹���ɵȵȣ�ע��ƽʱ��֪ʶ���ۣ�

��ϰ��ϵ�д�
�����Ŀ
�����з�Ӧ�����У���1mol����ת�Ƶ��ǣ�������
| A��1mol����ˮ��Ӧ |
| B��27g�����������ᷴӦ |
| C��22.4L��������״����������þ��Ӧ |
| D��1.5mol Na2O2������ˮ��Ӧ |


 �����Է�ˮ�������������ط���ȥ����ԭ����ͼ2��ʾ
�����Է�ˮ�������������ط���ȥ����ԭ����ͼ2��ʾ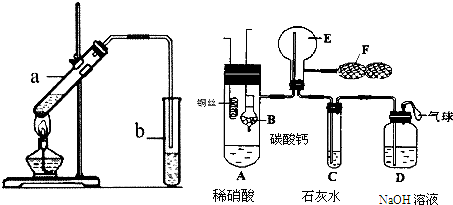

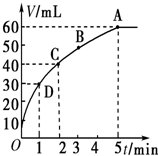 l mol MnO2��ĩ����50mL�����������Һ���=1.1g?L-1�����ڱ�״���£��ų���������y��ʱ��t�Ĺ�ϵ������ͼ��ʾ��
l mol MnO2��ĩ����50mL�����������Һ���=1.1g?L-1�����ڱ�״���£��ų���������y��ʱ��t�Ĺ�ϵ������ͼ��ʾ��