题目内容
一定条件下:4NH3+3F2═NF3+3NH4F,下列说法中正确的是( )
| A、氧化剂与还原剂的物质的量之比为3:4 |
| B、若反应消耗4mol NH3,则共转移12mol电子 |
| C、氧化产物与还原产物的物质的量之比为1:3 |
| D、NH4F不稳定,受热易分解 |
考点:氧化还原反应
专题:
分析:4NH3+3F2=NF3+3NH4F中,N元素的化合价由-3价升高为+3价,F元素的化合价由0降低为-1,以此来解答.
解答:
解:A.反应中,F2为氧化剂,NH3为还原剂,但NH3没有全部参加氧化反应,氧化剂与还原剂的物质的量之比为3:1,故A错误;
B.N元素的化合价由-3价升高为+3价,该反应中若反应消耗4mol NH3,得到1 mol NF3 时,转移1mol×[3-(-3)]=6 mol电子,故B错误;
C.该反应中只有1molNH3作还原剂,被氧化,3molF2作氧化剂被还原,NF3既是氧化产物也是还原产物,比值应为1:4,故C错误;
D.结合氯化铵的性质可知,NH4F不稳定,受热易分解,故D正确.
故选D.
B.N元素的化合价由-3价升高为+3价,该反应中若反应消耗4mol NH3,得到1 mol NF3 时,转移1mol×[3-(-3)]=6 mol电子,故B错误;
C.该反应中只有1molNH3作还原剂,被氧化,3molF2作氧化剂被还原,NF3既是氧化产物也是还原产物,比值应为1:4,故C错误;
D.结合氯化铵的性质可知,NH4F不稳定,受热易分解,故D正确.
故选D.
点评:本题综合考查氧化还原反应知识,侧重于氧化剂、氧化剂的判断、电子转移的数目的计算等问题,题目难度中等,注意从化合价变化的角度分析氧化还原反应.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
可用来提取含有杂质Br2的溴苯的试剂是( )
| A、水 | B、酒精 |
| C、NaOH溶液 | D、苯 |
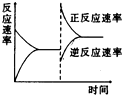 如图是改变某一外界条件后反应A2(s)+3B2(g)?2C(g)△H<0的反应速率与时间图象,则改变的条件可能是( )
如图是改变某一外界条件后反应A2(s)+3B2(g)?2C(g)△H<0的反应速率与时间图象,则改变的条件可能是( )| A、升高温度,同时加压 |
| B、保持体系压强不变加入反应物A2 |
| C、降低温度,同时减压 |
| D、保持体系压强不变加入反应物B2 |
铜片和锌片用导线连接后插入稀硫酸中构成原电池,正确的是( )
| A、铜片做负极发生氧化反应 |
| B、锌片做负极发生氧化反应 |
| C、铜片做阳极发生还原反应 |
| D、锌片做阴极发生还原反应 |
在与Al反应能产生H2的溶液中,一定可以大量共存的离子组是( )
| A、NH4+、Al3+、Br-、SO42- |
| B、Na+、Mg2+、Cl-、NO3- |
| C、K+、Ba2+、ClO-、NO3- |
| D、K+、Na+、I-、SO42- |
下列沸点最高的是( )
| A、正戊烷 | B、异戊烷 |
| C、丁烷 | D、丙烷 |
有下列物质:①白磷;②金刚石;③石墨;④二氧化硅;⑤甲烷;⑥四氯化碳;⑦单质硅;⑧铵根离子.其分子结构或晶体结构单元中存在正四面体的是( )
| A、除③外 | B、①②⑤⑥ |
| C、除③⑧外 | D、除③④⑦⑧ |
如图表示1~18号元素原子的结构或性质随核电荷数递增的变化.图中纵坐标表示( )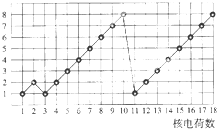

| A、最外层电子数 | B、原子半径 |
| C、最高化合价 | D、电子层数 |