题目内容
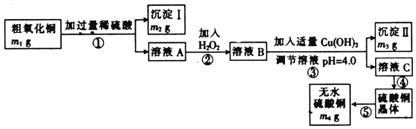
为测定粗氧化铜(其中含少量氧化亚铁及不溶于酸的杂质)中CuO的质量分数,并制取无水硫酸铜,某化学活动小组进行了下列实验:

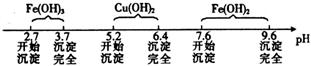
已知Fe3+、Cu2+、Fe2+三种离子在溶液中形成氢氧化物沉淀的pH范围如下:

请回答下列问题:
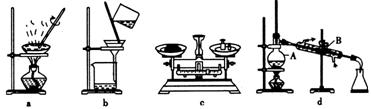
(1)在整个实验过程中,下列实验装置不可能用到的是

(2)溶液A中所含溶质的化学式为
(3)步骤②发生反应的离子方程式为
(4)沉淀II的化学式为
(5)粗氧化铜样品中CuO的质量分数为
×100%
×100%.(列出计算式)

已知Fe3+、Cu2+、Fe2+三种离子在溶液中形成氢氧化物沉淀的pH范围如下:

请回答下列问题:
(1)在整个实验过程中,下列实验装置不可能用到的是
d
d
(填字母),装置d中仪器A和B的名称分别为蒸馏烧瓶,冷凝管
蒸馏烧瓶,冷凝管
.
(2)溶液A中所含溶质的化学式为
FeSO4、CuSO4、H2SO4
FeSO4、CuSO4、H2SO4
.(3)步骤②发生反应的离子方程式为
2Fe2++H2O2+2H+=2Fe3++2H2O
2Fe2++H2O2+2H+=2Fe3++2H2O
.(4)沉淀II的化学式为
Fe(OH)3
Fe(OH)3
.(5)粗氧化铜样品中CuO的质量分数为
m1-m2-
| ||
| m1 |
m1-m2-
| ||
| m1 |
分析:(1)称量一定质量的药品用到托盘天平,本实验还有过滤和蒸发操作,没用到蒸馏;
(2)根据物质的性质和药品的用量来分析;
(3)根据物质的性质结合质量守恒定律、电荷守恒、氧化还原反应得失电子守恒等角度书写离子方程式;
(4)分析表中数据,根据物质的性质判断沉淀成分;
(5)根据质量守恒,利用关系式法计算质量分数;
(2)根据物质的性质和药品的用量来分析;
(3)根据物质的性质结合质量守恒定律、电荷守恒、氧化还原反应得失电子守恒等角度书写离子方程式;
(4)分析表中数据,根据物质的性质判断沉淀成分;
(5)根据质量守恒,利用关系式法计算质量分数;
解答:解:(1)实验中用到的化学操作有称量、过滤和蒸发,没有蒸馏操作,蒸馏用到的仪器有蒸馏烧瓶、冷凝管、牛角管、接收器以及酒精灯和铁架台等.
故答案为:d;蒸馏烧瓶,冷凝管;
(2)氧化铜和氧化亚铁分别与硫酸反应生成硫酸铜和硫酸亚铁,又硫酸过量,故答案为:FeSO4、CuSO4、H2SO4;
(3)Fe2+具有还原性,H2O2具有氧化性,二者在酸性条件下发生氧化还原反应生成Fe3+和H2O,故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;(4)Fe(OH)3;
(5)沉淀II为Fe(OH)3,根据铁元素守恒:FeO~FeSO4~Fe(OH)3,可知FeO的质量应为:
,所以CuO的质量为:m1-m2-
,
粗氧化铜样品中CuO的质量分数为
×100%,故答案为:
×100%.
故答案为:d;蒸馏烧瓶,冷凝管;
(2)氧化铜和氧化亚铁分别与硫酸反应生成硫酸铜和硫酸亚铁,又硫酸过量,故答案为:FeSO4、CuSO4、H2SO4;
(3)Fe2+具有还原性,H2O2具有氧化性,二者在酸性条件下发生氧化还原反应生成Fe3+和H2O,故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;(4)Fe(OH)3;
(5)沉淀II为Fe(OH)3,根据铁元素守恒:FeO~FeSO4~Fe(OH)3,可知FeO的质量应为:
| 72×m3 |
| 107 |
| 72×m3 |
| 107 |
粗氧化铜样品中CuO的质量分数为
m1-m2-
| ||
| m1 |
m1-m2-
| ||
| m1 |
点评:本题为物质的组成探究题,做题时注意分析生成流程,掌握物质的性质和实验基本操作,本题难度一般.

练习册系列答案
相关题目
 制取无水硫酸铜,某化学活动小组进行了下列实验:
制取无水硫酸铜,某化学活动小组进行了下列实验:




