题目内容
18.用双线桥法分析下列反应,并指明氧化剂、还原剂、氧化产物、还原产物.3Cu+8HNO3═Cu(NO3)2+2NO↑+4H2O
氧化剂:HNO3;还原剂:Cu;
氧化产物:Cu(NO3)2;还原产物:NO2.
分析 反应中化合价升高元素是Cu,所以反应物Cu是还原剂,化合价降低的是N元素,所以反应物HNO3是氧化剂,转移电子数为2,以此解答该题.
解答 解:反应方程式Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,中化合价变化为:Cu→Cu(NO3)2,Cu元素由0价→+2价,一个Cu原子失2个电子,所以Cu是还原剂,具有还原性,被氧化得到氧化产物为Cu(NO3)2;HNO3→NO2,N元素由+5价→+4价,一个HNO3分子得一个电子,所以HNO3是氧化剂,具有氧化性,被还原得到还原产物为NO2;其得失电子数为2,所以其转移电子数为2,即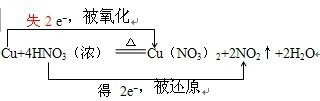 ;
;
故答案为: ;HNO3;Cu; Cu(NO3)2; NO2.
;HNO3;Cu; Cu(NO3)2; NO2.
点评 本题考查氧化还原反应,为高频考点,侧重于基本概念、电子转移表示方法的考查,难度不大,注意对基础知识的理解掌握.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
8.分类法在化学学科发展中起到了非常重要的作用,下列分类标准合理的是( )
| A. | 根据是否含有氧元素,将物质分为氧化剂和还原剂 | |
| B. | 根据是否具有丁达尔现象,将分散系分为溶液、胶体和浊液 | |
| C. | 根据水溶液是否能够导电,将物质分为电解质和非电解质 | |
| D. | 根据反应前后是否有元素化合价变化,可将化学反应分为氧化还原反应和非氧化还原反应 |
6.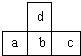 如图是周期表中短周期的一部分,若a原子最外层的电子数比次外层少了3个,则下列说法不正确的是( )
如图是周期表中短周期的一部分,若a原子最外层的电子数比次外层少了3个,则下列说法不正确的是( )
 如图是周期表中短周期的一部分,若a原子最外层的电子数比次外层少了3个,则下列说法不正确的是( )
如图是周期表中短周期的一部分,若a原子最外层的电子数比次外层少了3个,则下列说法不正确的是( )| A. | a、b、c的最高价氧化物对应水化物的酸性强弱的关系是c>b>a | |
| B. | d的氢化物比b的氢化物稳定 | |
| C. | d与c不能形成化合物 | |
| D. | 原子半径的大小顺序是a>b>c>d |
13.在托盘天平右盘上放一个盛有100mL3mol•L-1NaOH溶液的烧杯,左盘上放一个盛有100mL3mol•L-1盐酸的烧杯,调节天平至平衡,然后在两烧杯中各加入等质量2.7g的铝片,反应完全后,则天平可能出现的情况是( )
| A. | 左盘上升 | B. | 右盘下沉 | C. | 仍保持平衡 | D. | 无法判断 |
3.下列关于物质分类的说法正确的是( )
| A. | 金刚石、白磷都属于单质 | B. | 漂白液、石英都属于纯净物 | ||
| C. | 纯碱、烧碱都是碱 | D. | 蔗糖、蛋白质都属于高分子化合物 |
10.下列物质互为同分异构体的一组是( )
| A. | 35Cl和37Cl | B. | O2和O3 | ||
| C. | CH3CH2OH和CH3OCH3 | D. | 甲烷和丁烷 |
8.下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是( )
| A. | Cu(OH)2与盐酸 Cu(OH)2与醋酸 | |
| B. | BaCl2溶液与Na2SO4溶液 Ba(OH)2溶液与Na2SO4溶液 | |
| C. | NaHCO3溶液与NaHSO4溶液 Na2CO3溶液与NaHSO4溶液 | |
| D. | 石灰石与硝酸 生石灰与盐酸 |