题目内容
配制一定物质的量浓度的KOH溶液时,造成最终浓度偏低的原因可能是( )
| A、容量瓶事先未烘干 |
| B、称量KOH时天平砝码已生锈 |
| C、定容时观察液面仰视 |
| D、未冷却至室温就移液定容 |
考点:配制一定物质的量浓度的溶液
专题:物质的量浓度和溶解度专题
分析:分析不当操作对溶质的物质的量和溶液体积的影响,依据C=
进行误差分析.
| n |
| V |
解答:
解:A.容量瓶事先未烘干,对溶质的物质的量和溶液体积的影响都不会产生影响,溶液的浓度不变,故A不选;
B.称量KOH时天平砝码已生锈,导致称量的溶质的质量增大,溶质的物质的量偏大,溶液的浓度偏大,故B 不选;
C.定容时观察液面仰视,导致溶液的体积偏大,溶液的浓度偏低,故C选;
D.未冷却至室温就移液定容,冷却后溶液的体积偏小,溶液的浓度偏高,故D不选;
故选:C.
B.称量KOH时天平砝码已生锈,导致称量的溶质的质量增大,溶质的物质的量偏大,溶液的浓度偏大,故B 不选;
C.定容时观察液面仰视,导致溶液的体积偏大,溶液的浓度偏低,故C选;
D.未冷却至室温就移液定容,冷却后溶液的体积偏小,溶液的浓度偏高,故D不选;
故选:C.
点评:本题考查配制一定物质的量浓度溶液的误差分析,明确配制原理,依据C=
进行误差分析是解题关键,题目难度不大.
| n |
| V |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
只用水就能鉴别的一组物质是( )
| A、苯酚、乙醇、甘油 |
| B、乙醇、己烯、苯磺酸 |
| C、乙醛、乙二醇、硝基苯 |
| D、苯、乙醇、四氯化碳 |
实验中需2mol/L的Na2CO3溶液950mL,配制时应选用的容量瓶的规格和称取Na2CO3的质量分别是( )
| A、1000mL,212g |
| B、950mL,543.4g |
| C、950mL,572g |
| D、500mL,286g |
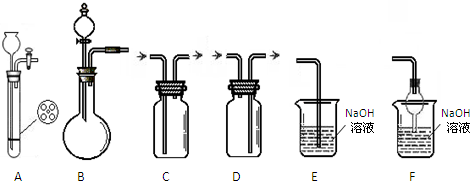
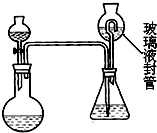
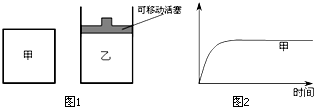 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,工业上合成氨反应通常用铁触媒作催化剂,反应方程式为:N2+3H2?2NH3△H<0.
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,工业上合成氨反应通常用铁触媒作催化剂,反应方程式为:N2+3H2?2NH3△H<0.